



版權說明:本文檔由用戶提供并上傳,收益歸屬內容提供方,若內容存在侵權,請進行舉報或認領
文檔簡介
專題4
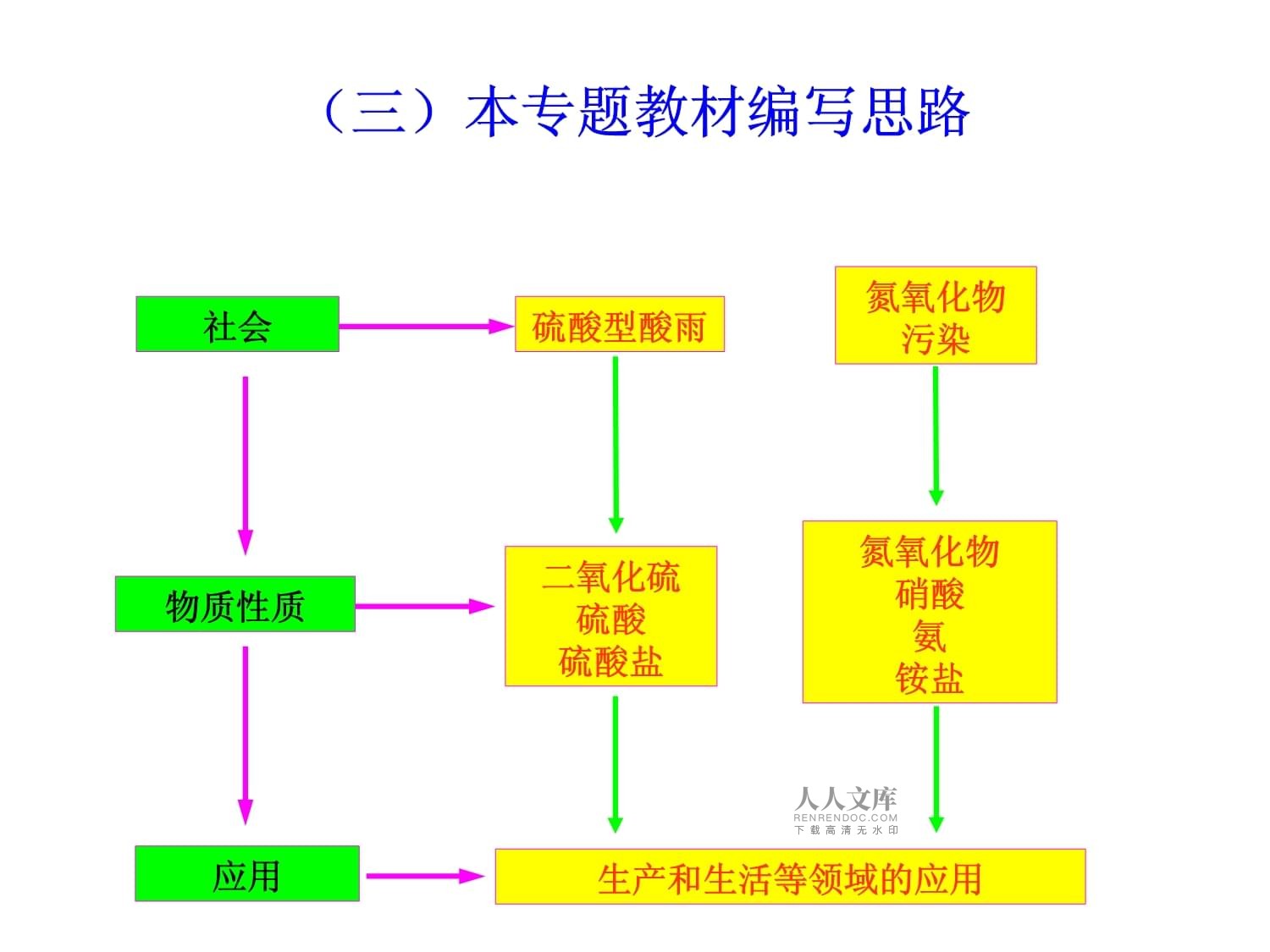
硫、氮和可持續發展復習社會物質性質應用硫酸型酸雨氮氧化物污染二氧化硫硫酸硫酸鹽氮氧化物硝酸氨銨鹽生產和生活等領域的應用(三)本專題教材編寫思路三、硫酸型酸雨的形成及防治SO2+H2OH2SO32SO2+O22SO3催化劑SO3+H2O=H2SO42H2SO3+O2
=2H2SO4硫酸型酸雨的形成酸雨:PH值小于5.6的降水。三、酸雨的形成及防治氨水法石灰石-石膏法Ca(OH)2+SO2=H2O+CaSO32CaSO3+O2=2CaSO4SO2+2NH3+H2O=(NH4)2SO32(NH4)2SO3+O2=(NH4)2SO4SO2+CaO=CaSO3
△2CaSO3+O2=2CaSO4
△CaCO3=CO2↑+CaO△3.你認為減少酸雨產生的途徑可采用的措施是______________。①少用煤作燃料;②把工廠煙囪造高;③燃料脫硫;④在已酸化的土壤中加石灰;⑤開發新能源。①③⑤例題.A、B兩種氣體都是污染大氣的主要污染物,國家《環境保護法》嚴禁未經處理就把它們排放到空氣中。A是一種單質,其水溶液具有殺菌消毒作用,B是形成酸雨的主要污染物。請寫出下列變化的化學方程式:⑴A用于工業上制取漂白精:
;⑵B的水溶液露置在空氣中酸性增強:
;⑶A、B都能分別使品紅試液褪色,但兩者水溶液混合后卻不能使品紅褪色且溶液酸性增強:
;2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O2H2SO3+O2=2H2SO4Cl2+SO2+2H2O=H2SO4+2HClSO2與H2O反應與堿反應氧化性還原性酸性氧化物+4價漂白性特性重視環境保護,防止酸雨危害環境!與堿性氧化物SO2+2NaOH=Na2SO3+H2OSO2+Cl2+2H2O=H2SO4+2HClSO2+2Br2+2H2O=H2SO4+2HBrSO2+2H2S=3S↓+2H2O品紅褪色,加熱后又變紅課堂練習下列可以用來鑒別SO2
和CO2
的方法是[]A、通入紫色石蕊試液B、聞氣味
C、通入澄清石灰水D、通入品紅溶液中都是酸性氧化物,都可以使石蕊變紅SO2有刺激性氣味,而CO2沒有都可以使澄清石灰水變渾濁SO2可使品紅褪色,而CO2不能BD1、下列關于SO2的說法中錯誤的是()
A.SO2是一種無色,有刺激性氣味的有毒氣體
B.SO2能使紫色的石蕊變紅色
C.SO2是硫酸的酸酐,稱為硫酐
D.SO2能與CaO反應生成CaSO3C2、下列物質做干燥劑可干燥SO2的是()
A.生石灰
B.NaOH固體
C.堿石灰
D.濃硫酸D5.銀耳本身為淡黃色,福建省生產的一種雪耳,顏色潔白如雪。其制作過程如下:將銀耳堆放在密閉狀態良好的塑料棚內,在棚的一端支一口小鍋,鍋內放有硫磺,加熱使硫磺融化并燃燒,兩天左右,雪耳就制成了,雪耳燉而不爛,且對人體有害,制作雪耳利用的就是()A.硫的還原性B.硫的漂白性C.二氧化硫的還原性D.二氧化硫的漂白性D“硫酸的制備和性質”知識體系硫酸FeS2(或S)SO2SO3稀硫酸的通性濃硫酸的特性吸水性脫水性氧化性工業制硫酸的原理硫酸的性質及應用1、一瓶濃鹽酸和一瓶濃硫酸長期敞口放置,質量會如何變化?濃度如何變化?2、硫酸在下列用途或反應中各表現的性質是:
A.強酸性B.難揮發性C.吸水性D.脫水性
E.強氧化性F.高沸點性(1)干燥H2、SO2等氣體________;(2)用鋁槽車裝運濃硫酸________;(3)清洗鍍件表面氧化物________;(4)濃硫酸使濕潤石蕊試紙變紅,后來又變黑_____(5)膽礬中加入濃硫酸,久置變為白色粉末
;(6)蔗糖中加入濃硫酸,形成“黑色發糕”
;濃鹽酸質量減少,濃硫酸質量增加。濃度均減小。CEAAECDE一、硫酸工業生產的原理第一步:硫磺(或含硫礦石)與氧氣反應生成SO2S+O2=SO2點燃沸騰爐4FeS2+11O2=2Fe2O3+8SO2高溫第二步:SO2在催化劑作用下與氧氣反應生成SO3接觸室第三步:SO3的吸收SO3+H2OH2SO4吸收塔2SO2+O22SO3催化劑△硫酸工業生產流程動畫硫酸的工業生產沸騰爐接觸室吸收塔凈化冷卻21.下列說法正確的是A工業制取硫酸的設備依次是沸騰爐、熱交換器、吸收塔。B硅是制造光導纖維的材料C水玻璃是建筑行業常用的一種黏合劑。D純堿、石灰石是制取水泥的原料C“硫及其化合物之間的相互轉化”知識體系Na2SO4H2SO4BaSO4SO3SO2SH2SFeSHgSH2SO3Na2SO3不同價態硫元素之間的氧化還原反應及含同價態硫元素的物質之間的酸堿反應4.下列物質均有漂白作用,其漂白原理相同的是()①雙氧水②次氯酸③二氧化硫④活性炭⑤臭氧A.①②⑤B.①③⑤C.②③④D.①②③A“氮氧化合物的產生及轉化”知識體系①雷電(自然固氮)NONO2HNO3空氣中N2②化工、汽車尾氣雷雨發莊稼光化學煙霧32O
NO2
23O主要反應拓展N2+3H22NH3催化劑高溫高壓“氮肥的生產和使用”知識體系空氣中N2NH3溶解性NH4+弱堿性氯化銨的熱分解銨鹽與堿反應空氣合成氨的意義銨態氮肥使用性質探究銨態氮肥NH4+的檢驗:溶液中加入NaOH共熱,濕潤的紅色石蕊試紙變藍。NH4++OH-=NH3+H2O氮肥的生產和使用
1、氨氣(2)性質:2、銨鹽(1)生產:(3)制取:易溶于水;一元弱堿。(1)易溶解;(2)易分解;(2)易堿解。“硝酸的性質”知識體系NH3NONO2HNO3物理性質不穩定性、強酸性強氧化性(濃、稀硝酸與銅反應,濃硝酸與炭反應,鈍化)硝酸工業制法硝酸的性質及應用Cu+4HNO3(濃)Cu(NO3)2+2NO2↑+2H2O3Cu+8HNO3(稀)3Cu(NO3)2+2NO↑+4H2OC+4HNO3(濃)==CO2↑
+4NO2↑+2H2O△S+6HNO3(濃)H2SO4+6NO2↑+2H2O
△4HNO32H2O+4NO2↑+O2↑
△或光照足量的Cu中加入少量的濃硝酸,可能會發生什么反應?
反應停止后,如果在溶液中再加入足量鹽酸,會出現什么情況?溶液中存在NO3-,它遇到H+后,會繼續氧化銅,當然此時NO3-/H+的溶度較稀.思考題
一開始是銅與濃硝酸反應:Cu+4HNO3(濃)Cu(NO3)2+2NO2↑+2H2O隨著反應進行,硝酸由濃變稀,則發生:3Cu+8HNO3(稀)3Cu(NO3)2+2NO↑+4H2O思考題1、工業上擬用Cu與適量的硝酸來制備Cu(NO3)2,下面是三位同學提出的三個方案:甲:銅濃硝酸乙:銅稀硝酸丙:銅空氣△硝酸請問:那一種方案最好?為什么?Cu(NO3)2Cu(NO3)2Cu(NO3)2CuOA、B、C、D五種物質按右圖所示發生轉變(反應條件已略去)。(1)若A在通常情況下是固體,則A、B、C、D、E的化學式分別是:A
B
C
D
E
,(2)若A在通常情況下是氣體,則A、B、C、D、E的化學式分別是:A
B
C
D
E
、
SSO3SO2H2SH2SO4N2NO2NONH3HNO32.環境污染問題越來越受到人們的關注,造成環境污染的主要原因大多是由于人類生產活動中過度排放有關物質引起的。下列環境問題與所對應的物質不相關的是 ()
A.溫室效應——二氧化碳
B.光化學污染——二氧化氮
C.酸雨——二氧化碳
D.臭氧層破壞——氟氯烴CA、B、C、D、E是含有一種相同元素的五種物質,在一定條件下可發生如下圖所示的轉化,其中A是單質,B是氣體,C、D是氧化物,E是最高價氧化物對應的水化物,則A可能是()A.Cl2B.N2C.SD.CABCDEBC
4.最新的研究表明:一氧化氮吸入治療法可快速改善SARS中重癥患者的缺氧狀況,緩解病情。病毒學研究證實,一氧化氮對SARS病毒有直接抑制作用。下列關于一氧化氮的敘述正確的是()
A.一氧化氮是一種紅棕色的氣體
B.常溫常壓下,一氧化氮不能與空氣中的氧氣直接化合
C.含等質量氧元素的一氧化氮與一氧化碳的物質的量相等
D.一氧化氮易溶于水,不能用排水法收集
C下圖A~H分別代表有關反應中的一種物質,其中B是能使澄清石灰水變渾濁的無色無味的氣體,完成以下空白:(1)A、B、C的化學式分別是
、
、
。(2)C與氧氣反應的化學方程式是
。(3)G與C反應的化學方程式是
。NH4HCO3CO2NH3NONO2NOHNO3(NH4)2CO3H2O16.(8分)右圖是某元素及其重要化合物的相互轉化關系圖(生成物中不含該元素的物質均已略去),圖中A是單質,D在常溫下呈氣態,F可用作氮肥,也可用來作炸藥。(1)寫出A和F的化學式:A
、F
;
(2)寫出下列變化的化學方程式:
B→C:
。
E→C:
。NO2
溫馨提示
- 1. 本站所有資源如無特殊說明,都需要本地電腦安裝OFFICE2007和PDF閱讀器。圖紙軟件為CAD,CAXA,PROE,UG,SolidWorks等.壓縮文件請下載最新的WinRAR軟件解壓。
- 2. 本站的文檔不包含任何第三方提供的附件圖紙等,如果需要附件,請聯系上傳者。文件的所有權益歸上傳用戶所有。
- 3. 本站RAR壓縮包中若帶圖紙,網頁內容里面會有圖紙預覽,若沒有圖紙預覽就沒有圖紙。
- 4. 未經權益所有人同意不得將文件中的內容挪作商業或盈利用途。
- 5. 人人文庫網僅提供信息存儲空間,僅對用戶上傳內容的表現方式做保護處理,對用戶上傳分享的文檔內容本身不做任何修改或編輯,并不能對任何下載內容負責。
- 6. 下載文件中如有侵權或不適當內容,請與我們聯系,我們立即糾正。
- 7. 本站不保證下載資源的準確性、安全性和完整性, 同時也不承擔用戶因使用這些下載資源對自己和他人造成任何形式的傷害或損失。

評論
0/150
提交評論