



版權(quán)說明:本文檔由用戶提供并上傳,收益歸屬內(nèi)容提供方,若內(nèi)容存在侵權(quán),請進行舉報或認領(lǐng)
文檔簡介
1、年 級高三學(xué) 科化學(xué)版 本人教新課標(biāo)版課程標(biāo)題高考第一輪復(fù)習(xí)幾種重要的金屬鐵和鋁編稿老師劉學(xué)超一校林卉二校黃楠審核張美玲一、考綱要求1. 了解鐵和鋁的單質(zhì)及其重要化合物的主要性質(zhì)和應(yīng)用。2. 以Fe2和 Fe3的相互轉(zhuǎn)化為例,理解變價金屬元素的氧化性和還原性。3. 了解合金的概念及其重要應(yīng)用。二、考題規(guī)律:金屬單質(zhì)及其化合物的知識,在高考中占有重要的地位,每年必考,試題形式多樣,選擇、簡答、實驗、推斷、計算題都有。考查的知識點有:1. Al3、AlO、Al(OH)3之間的相互轉(zhuǎn)化及有關(guān)沉淀量變化的計算;鐵及其化合物的知識點較多,高考命題時往往將實驗、理論、化學(xué)常識及概念的考查集于一身,設(shè)計成具
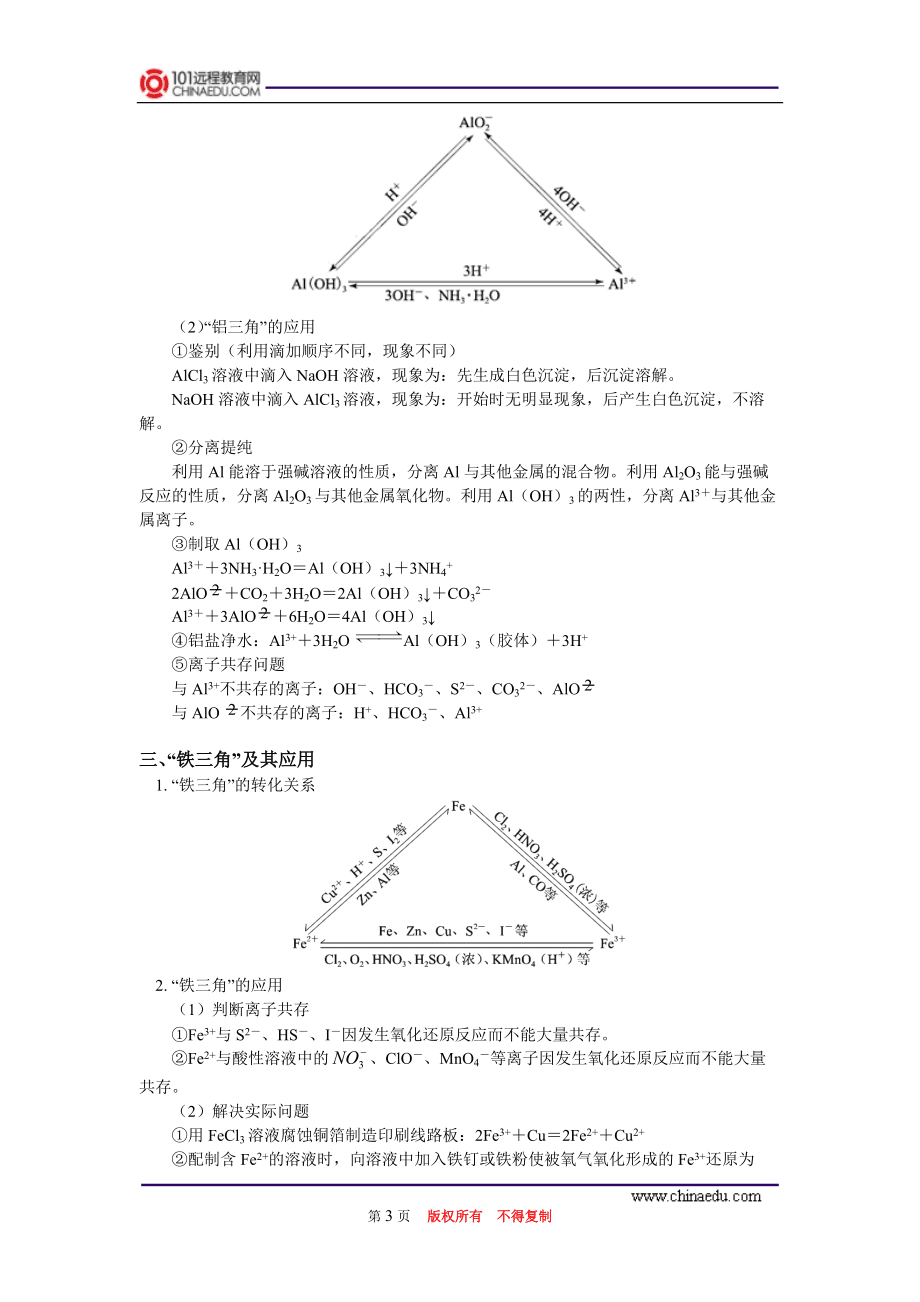
2、有一定綜合性的題目;2. 鐵的三種價態(tài)的相互轉(zhuǎn)化關(guān)系;3. Fe3的氧化性、Fe2的還原性,F(xiàn)e2和 Fe3+的鑒別方法;4. 鐵的合金及鋼鐵的腐蝕與防護。三、考向預(yù)測:在今后的高考中,題型會穩(wěn)中有變,以鐵和鋁及其化合物的知識為依托的無機推斷仍是主要的考查方式,也會與解釋現(xiàn)象、定性推斷、歸納總結(jié)、定量計算相結(jié)合。同時側(cè)重化學(xué)用語及方程式的考查,金屬單質(zhì)及其化合物知識與化學(xué)理論知識、基本概念、實驗有著廣泛的聯(lián)系,實際應(yīng)用也很廣泛,命題空間極為廣闊,能較全面地考查出學(xué)生的學(xué)科能力,符合高考命題的發(fā)展趨勢,在復(fù)習(xí)中應(yīng)注意強化與之相關(guān)的基礎(chǔ)知識。一、鐵、鋁及其化合物轉(zhuǎn)化關(guān)系:要點展示:二、“鋁三角”的
3、轉(zhuǎn)化關(guān)系及其應(yīng)用 (1)“鋁三角”的轉(zhuǎn)化關(guān)系(2)“鋁三角”的應(yīng)用 鑒別(利用滴加順序不同,現(xiàn)象不同) AlCl3溶液中滴入NaOH溶液,現(xiàn)象為:先生成白色沉淀,后沉淀溶解。 NaOH溶液中滴入AlCl3溶液,現(xiàn)象為:開始時無明顯現(xiàn)象,后產(chǎn)生白色沉淀,不溶解。 分離提純 利用Al能溶于強堿溶液的性質(zhì),分離Al與其他金屬的混合物。利用Al2O3能與強堿反應(yīng)的性質(zhì),分離Al2O3與其他金屬氧化物。利用Al(OH)3的兩性,分離Al3與其他金屬離子。制取Al(OH)3Al33NH3·H2OAl(OH)33NH4+ 2AlOCO23H2O2Al(OH)3CO32Al33AlO6H2O4Al(
4、OH)3鋁鹽凈水:Al3+3H2OAl(OH)3(膠體)3H+離子共存問題與Al3+不共存的離子:OH、HCO3、S2、CO32、AlO與AlO不共存的離子:H+、HCO3、Al3+三、“鐵三角”及其應(yīng)用1. “鐵三角”的轉(zhuǎn)化關(guān)系2. “鐵三角”的應(yīng)用(1)判斷離子共存Fe3+與S2、HS、I因發(fā)生氧化還原反應(yīng)而不能大量共存。 Fe2+與酸性溶液中的、ClO、MnO4等離子因發(fā)生氧化還原反應(yīng)而不能大量共存。 (2)解決實際問題 用FeCl3溶液腐蝕銅箔制造印刷線路板:2Fe3+Cu2Fe2+Cu2+ 配制含F(xiàn)e2+的溶液時,向溶液中加入鐵釘或鐵粉使被氧氣氧化形成的Fe3+還原為Fe2+:2Fe
5、3+Fe3Fe2+。配制Fe3的鹽溶液:加少量相應(yīng)的酸防止Fe3水解。 人體只能吸收Fe2+,維生素C可將Fe3+還原成Fe2+,適量服用維生素C有利于鐵元素的吸收。 為除去廢水中的Fe2+,常先將廢水中的Fe2+氧化為Fe3+,再調(diào)節(jié)溶液的pH使Fe3+轉(zhuǎn)化為Fe(OH)3沉淀析出。制取Fe(OH)3(膠體):Fe33H2O(沸水)Fe(OH)3(膠體)3H制備無水FeCl3:FeCl3·6H2OFeCl36H2O(3)Fe3+、Fe2+的檢驗方法1: 方法2:KSCN溶液和氯水法方法3:NaOH溶液法有關(guān)反應(yīng)的方程式:Fe22OHFe(OH)2 4Fe(OH)22H2OO24Fe
6、(OH)3Fe33OHFe(OH)3聚焦熱點1:鋁及其化合物例1 鋁土礦的主要成分為氧化鋁、氧化鐵和二氧化硅,工業(yè)上經(jīng)過下列工藝可以冶煉金屬鋁:下列說法中錯誤的是( )A. 中除加試劑外,還需要進行過濾操作 B. a、b中鋁元素的化合價相同C. 中需要通入過量的氨氣 D. 進行的操作是加熱,而且d一定是氧化鋁分析:反應(yīng)后的體系中含有固體二氧化硅,需要過濾除去,反應(yīng)后的體系中有氫氧化鐵沉淀,需要過濾除去,A正確;a、b中的鋁元素分別以AlCl3和NaAlO2的形式存在,其中鋁的化合價都是3,B正確;由偏鋁酸鈉制備氫氧化鋁需要通入過量二氧化碳,C錯;由氫氧化鋁制備氧化鋁,加熱即可,D正確。答案:C
7、點評:這道題重點考查了有關(guān)鋁及其化合物的主要化學(xué)性質(zhì)。希望同學(xué)們重點把握好Al(OH)3是兩性的氫氧化物其可溶于強堿和強酸,但不溶于弱堿和弱酸。例2 甲、乙兩燒杯中分別裝有體積相同、pH相同的氨水和NaOH溶液,各加入10 mL 0.1 mol·L1的AlCl3溶液,兩燒杯中都有沉淀生成。下列判斷正確的是( )A. 甲中沉淀一定比乙中的多 B. 甲中沉淀可能比乙中的少C. 甲中沉淀一定比乙中的少 D. 甲中和乙中的沉淀可能一樣多分析:根據(jù)氫氧化鋁的性質(zhì),其能溶于氫氧化鈉但不溶于氨水。體積相同、pH相同的兩溶液中的溶質(zhì)物質(zhì)的量氨水大于氫氧化鈉,當(dāng)兩者均不足量時,生成的沉淀氨水多;氨水過
8、量,氫氧化鈉不足量時,生成的沉淀氨水多;氨水過量,氫氧化鈉恰好時,生成的沉淀一樣多;氨水和氫氧化鈉都過量時,生成的沉淀氨水多;可知D正確。答案:D點評:解答此題時,選用的是討論法,其多用于計算條件不足的題,據(jù)此求解時需要在分析推理的基礎(chǔ)上通過某些假設(shè)條件,再加以討論才能正確解答;故在應(yīng)用討論法解題時,關(guān)鍵是先要分析條件與求解問題之間的聯(lián)系,形成正確的解題方法。例3 某實驗小組對一含有Al3的未知溶液進行了定量分析,作出了滴入NaOH溶液體積與沉淀物質(zhì)的量之間關(guān)系的圖象。試回答下列問題:(1)該未知溶液中至少含有_種陽離子。(2)滴加的NaOH溶液的物質(zhì)的量濃度為多少? (3)若該未知
9、溶液中只含三種陽離子且一種是二價陽離子,求a的值。分析:(1)從圖象可以看出,開始時無沉淀,說明有H離子,產(chǎn)生的沉淀部分溶解,說明至少有兩種離子能與OH作用,故該溶液中至少含有三種陽離子。(2)由Al(OH)3NaOHNaAlO22H2O可知,nAl(OH)3n(NaOH)0.20 mol0.15 mol0.05 mol,則c(NaOH)5 mol·L1。(3)nAl(OH)30.05 mol,則另一種沉淀nM(OH)20.15 mol,產(chǎn)生沉淀消耗的n(NaOH)0.05 mol×30.15 mol×20.45 mol,所以產(chǎn)生沉淀消耗的V(NaOH)0.09
10、L90 mL,故a100 mL90 mL10 mL。答案:(1)三 (2)5 mol · L1 (3)10點評:解決有關(guān)Al(OH)3沉淀的圖象題,其突破點往往就是沉淀量減少的一段,該段發(fā)生的反應(yīng)為:Al(OH)3NaOHNaAlO22H2O,即沉淀減少的物質(zhì)的量等于參加該段反應(yīng)的NaOH的物質(zhì)的量。聚焦熱點2:鐵及其化合物例1 能正確表示下列反應(yīng)的離子方程式是( )A. 將銅屑加入溶液中:B. 將磁性氧化鐵溶于鹽酸:C. 將氯化亞鐵溶液和稀硝酸混合:D. 將鐵粉加入稀硫酸中:分析:A正確,符合3個守恒;B錯誤,電荷不守恒,F(xiàn)e3O4中Fe有兩種價態(tài),正確的應(yīng)為:Fe3O48H2Fe
11、3Fe24H2O;C錯誤,得失電子不守恒,電荷不守恒;正確的應(yīng)為:3Fe2NO34H3Fe3NO2H2O;D錯誤,不符合客觀實際,反應(yīng)后鐵只能產(chǎn)生Fe2和H2。答案:A點評:離子方程式的正誤判斷是個老生常談的問題,但有關(guān)鐵及其化合物的離子方程式的問題,除了掌握基本的書寫原則以外,還要注意Fe2、Fe3的特殊性等問題。例2 下列反應(yīng)發(fā)生后一定有3價鐵生成的是( )過量的Fe與Cl2反應(yīng) Fe與過量的稀H2SO4反應(yīng)后,再向其中加入KNO3 向Fe(NO3)2溶液中加少量鹽酸 把Fe和Fe2O3的混合物溶于鹽酸中A. 只有 B. 只有 C. 只有 D. 全部分析:Fe與Cl2反應(yīng)一定生成FeCl3
12、,與反應(yīng)物的用量無關(guān);Fe與稀H2SO4反應(yīng)生成Fe2,F(xiàn)e2在酸性條件下被NO氧化成Fe3;一定生成Fe3;當(dāng)Fe過量時生成Fe2,當(dāng)Fe2O3過量時有Fe3生成,故C正確。答案:C點評:這道題重點考查了鐵以及Fe2的還原性問題,要注意的是生成Fe3需要的氧化劑應(yīng)其氧化性應(yīng)較強。同時注意Fe與FeCl3必須是在溶液中才能發(fā)生反應(yīng),NO3只有在酸性條件下才有氧化性。例3 下列敘述正確的是( ) A. 向某溶液中通入Cl2,然后再加入KSCN溶液變紅色,說明原溶液中含有Fe2 B. 向某溶液中加入NaOH溶液得白色沉淀,又觀察到顏色逐漸變?yōu)榧t褐色,說明該溶液中只含F(xiàn)e2,不含Mg2 C. 過量的
13、鐵粉投入到一定的稀硝酸中,充分反應(yīng)后取上層清液于試管中,滴加KSCN溶液,溶液顯紅色 D. 檢驗紅磚中的氧化鐵成分,向紅磚粉末中加入鹽酸,充分反應(yīng)后取上層清液于試管中,滴加KSCN溶液23滴即可分析:加入KSCN溶液變紅色,說明含F(xiàn)e3,但Cl2具有氧化性,故無法判斷原溶液中所含的是Fe2還是Fe3,A項錯誤;加入NaOH溶液得白色沉淀后變成紅褐色,說明含F(xiàn)e2,但由于紅褐色的掩蓋,無法說明是否含Mg2,B項錯誤;過量的鐵粉與稀硝酸反應(yīng)最終生成的是Fe2,C項錯誤;D項正確。答案:D 點評:檢驗Fe2和Fe3時要結(jié)合它們所處的溶液環(huán)境選擇合適的檢驗方法,如在Fe2和Fe3共存的溶液中檢驗Fe2
14、,就應(yīng)選用酸性KMnO4溶液,若KMnO4溶液的紫色褪去,則證明含有Fe2。聚焦熱點3:有關(guān)鋁及鐵元素的綜合試題例1 下圖AJ分別代表有關(guān)反應(yīng)中的一種物質(zhì),它們均為中學(xué)化學(xué)中的常見物質(zhì)。 已知AE和FJ中分別含有同一種元素。反應(yīng)EAO2的條件未標(biāo)出。 請?zhí)顚懴铝锌瞻祝?(1)化合物H中的陽離子是 (填離子符號)。 (2)A生成B反應(yīng)的離子方程式是 。 (3)A和F的混合物發(fā)生反應(yīng)的化學(xué)方程式是 (4)IJ反應(yīng)的化學(xué)方程式是 。分析:由AB和AC的轉(zhuǎn)化,可知A是既能與酸反應(yīng)又能與堿反應(yīng)的兩性物質(zhì),結(jié)合EAO2的反應(yīng)特點和AE含有同一種元素可推知:A為Al,B為偏鋁酸鹽,C為鋁鹽,D是Al(OH)
15、3,E是Al2O3。從而推出AFEG的反應(yīng)為“鋁熱反應(yīng)”,則G為金屬單質(zhì),F(xiàn)是金屬G的氧化物,H為含G陽離子的鹽,I是含G陽離子的鹽與OH反應(yīng)生成含G的氫氧化物,結(jié)合IJ的轉(zhuǎn)化關(guān)系(在空氣中可繼續(xù)被氧化)可知金屬G為變價金屬,從而可推知G應(yīng)為Fe;H中含有Fe2+;J為Fe(OH)3;F為Fe2O3。所以有關(guān)反應(yīng)的方程式分別為:AB的離子方程式:2Al2OH2H2O2AlO23H2;AFEG反應(yīng)的方程式為:;IJ反應(yīng)的方程式為:4Fe(OH)2O22H2O4Fe(OH)3。答案:(1)Fe2+(2)2Al2OH2H2O2AlO23H2 (3) (4)4Fe(OH)2O22H2O4Fe(OH)3
16、點評:無機框圖推斷題的解題關(guān)鍵是要找出目的題眼,也就是要找出解決問題的突破口。突破口往往是有關(guān)物質(zhì)的特性和有關(guān)的反應(yīng)條件。如這道題的題眼是:物質(zhì)的特性是:A是既能與酸反應(yīng)又能與堿反應(yīng)的兩性物質(zhì)。條件是:AFEG需要高溫,IJ的轉(zhuǎn)化需要在空氣中被氧化。例2 鋁是一種重要的金屬,在生產(chǎn)、生活中具有許多重要的用途,下圖是從鋁土礦中制備鋁的工藝流程:已知:(1)鋁土礦的主要成分是Al2O3,此外還含有少量SiO2、Fe2O3等雜質(zhì);(2)溶液中的硅酸鈉與偏鋁酸鈉反應(yīng),能生成硅鋁酸鹽沉淀,化學(xué)反應(yīng)方程式為:2Na2SiO32NaAlO22H2ONa2Al2Si2O84NaOH回答下列問題:(1)寫出向鋁
17、土礦中加入足量氫氧化鈉溶液后,該步操作中發(fā)生反應(yīng)的離子方程式:_.(2)濾渣A的主要成分為_;濾渣A的用途是_(只寫一種);實驗室過濾時使用玻璃棒,其作用是_。(3)在工藝流程的第三步中,選用二氧化碳作酸化劑的原因是 _.(4)若將鋁溶解,下列試劑中最好選用_(填編號)。A. 濃硫酸 B. 稀硫酸 C. 稀硝酸理由是_.分析:(1)Al2O3屬于兩性氧化物,SiO2屬于酸性氧化物,都能與強堿反應(yīng)。(2)利用題目給出的信息“硅鋁酸鹽沉淀”,可以知道濾渣A的主要成分是Fe2O3、Na2Al2Si2O8.對于濾渣A的用途一般很容易想到其可以作為煉鐵的原料。(3)因為Al(OH)3是兩性氫氧化物,若用
18、強酸酸化濾液時,無法保證將全部鋁元素轉(zhuǎn)化為Al(OH)3過濾出來。(4)分析問題時,一般要同時考慮生產(chǎn)效益(原料利用率)和環(huán)保問題。答案:(1)Al2O32OH2AlOH2O、 SiO22OHSiOH2O(2)Fe2O3、Na2Al2Si2O8 煉鐵的原料(或生產(chǎn)硅酸鹽產(chǎn)品的原料) 引流(3)經(jīng)過足量氫氧化鈉溶液的溶解,大部分鋁元素均以NaAlO2的形式存在于濾液中,通入過量二氧化碳可以將NaAlO2完全轉(zhuǎn)化為Al(OH)3(4)B 鋁與濃硫酸在常溫下發(fā)生鈍化,加熱溶解會產(chǎn)生有毒氣體SO2,原料利用率低;稀硝酸能溶解鋁,但會產(chǎn)生NO氣體,污染空氣,硝酸利用率低;而鋁與稀硫酸反應(yīng)速率較快,產(chǎn)生的
19、H2對空氣無污染點評:流程型題首先要明確試題的目的和要求,以及題目提供的有效信息。然后從各個環(huán)節(jié)中去尋找問題的突破口。一、鋁鹽與強堿溶液作用主要反應(yīng)關(guān)系有: Al33OHAl(OH)3 Al(OH)3OHAlO2H2O Al34OHAlO2H2O(1)定量分析可溶性鋁鹽與強堿(如NaOH溶液)反應(yīng),Al元素的存在形式(2)計算關(guān)系分析以上三個反應(yīng)關(guān)系式,所得Al(OH)3沉淀的物質(zhì)的量與n(Al3)、n(OH)的關(guān)系為:當(dāng)時,所得沉淀的物質(zhì)的量:nAl(OH)3n(OH);當(dāng)時,所得沉淀的物質(zhì)的量:nAl(OH)30;當(dāng)時,所得沉淀的物質(zhì)的量:nAl(OH)34n(Al3)n(OH)。二、鐵與
20、稀HNO3的反應(yīng)隨著兩者的量的不同,生成的氧化產(chǎn)物亦不同,可用討論的方法確定。Fe4HNO3(稀)Fe(NO3)3NO2H2OFe2Fe(NO3)33Fe(NO3)2×2可得:3Fe8HNO3(稀)3Fe(NO3)22NO4H2O當(dāng)時,硝酸過量,按式計算。當(dāng)時,鐵過量,按式計算。當(dāng)時,可依據(jù)式或式進行計算。無論二者的量如何變化,鐵與稀HNO3反應(yīng),被還原的HNO3與參加反應(yīng)的HNO3的物質(zhì)的量之比總是14。下一講我們復(fù)習(xí)的內(nèi)容是:無機非金屬材料的主角碳和硅。主要復(fù)習(xí):C、Si的單質(zhì)及其化合物的主要性質(zhì)及應(yīng)用。了解C、Si單質(zhì)及其化合物對環(huán)境質(zhì)量的影響以及該部分知識的綜合應(yīng)用。(答題時
21、間:60分鐘)一、選擇題(每小題僅有一個正確選項)1. 鋁具有較強的抗腐蝕性能,主要是因為( )A. 鋁性質(zhì)不活潑 B. 鋁能耐酸堿C. 鋁與氧氣常溫下不反應(yīng) D. 鋁表面形成一層氧化膜起保護作用2. 下列關(guān)于鐵的敘述正確的是( )鐵能被磁鐵吸引,但純鐵易銹蝕 在人體的血紅蛋白中含有鐵元素 鐵位于周期表中的第四周期第B族 鐵能在氧氣中劇烈燃燒,但不能在水蒸氣中燃燒 鐵與硝酸反應(yīng)的產(chǎn)物僅是Fe(NO3)3 不能通過化合反應(yīng)生成FeCl2和Fe(OH)3A. B. C. D. 3. 等量鎂鋁合金粉末分別與下列4種過量的溶液充分反應(yīng),放出氫氣最多的是( )A. 2 mol·L1H2SO4溶
22、液 B. 18 mol·L1H2SO4溶液C. 6 mol·L1KOH溶液 D. 3 mol·L1HNO3溶液4. 下列有關(guān)實驗的說法正確的是( )A. 除去鐵粉中混有的少量鋁粉,可加入過量的氫氧化鈉溶液,完全反應(yīng)后過濾B. 為測定熔融氫氧化鈉的導(dǎo)電性,可在瓷坩堝中熔化氫氧化鈉固體后進行導(dǎo)電性實驗C. 制備Fe(OH)3膠體,通常是將Fe(OH)3固體溶于熱水中D. 某溶液中加入鹽酸能產(chǎn)生使澄清石灰水變渾濁的氣體,則該溶液中一定含有CO5. 下列有關(guān)金屬鋁及其化合物的敘述正確的是( )A. 鋁在常溫下不能與氧氣反應(yīng) B. 鋁不能與氯氣反應(yīng)C. 鋁既能溶于酸,又能溶
23、于堿 D. 氧化鋁只能與酸反應(yīng),不能與堿反應(yīng)*6. 在硫酸鐵溶液中,加入a g銅,完全溶解后,又加入b g鐵,充分反應(yīng)后得到c g殘余固體,且b<c,則下列判斷正確的是( )A. 最后得到的溶液中含有Fe3 B. 殘余固體可能為鐵、銅的混合物C. 最后得到的溶液中只含Cu2 D. 殘余固體一定全部是銅7. 下列敘述正確的是( )A. 將CO2通入BaCl2溶液中至飽和,無沉淀產(chǎn)生;再通入SO2產(chǎn)生沉淀B. 在稀硫酸中加入銅粉,銅粉不溶解;再加入Cu(NO3)2固體,銅粉仍不溶解C. 向AlCl3溶液中滴加氨水,產(chǎn)生白色沉淀;再加入過量NaHSO4溶液,沉淀消失D. 純鋅與稀硫酸反應(yīng)產(chǎn)生氫
24、氣的速率較慢;再加入少量CuSO4固體,速率不改變*8. 某學(xué)生設(shè)計了如圖的方法對X鹽進行鑒定: 由此分析,下列結(jié)論中正確的是( )A. X中一定有Fe3 B. Z中一定有Fe3C. Y為AgI沉淀 D. X一定為FeBr2溶液*9. 將15.6 g Na2O2和5.4 g Al同時放入一定量的水中,充分反應(yīng)后得到200 mL溶液,再向該溶液中緩慢通入標(biāo)準(zhǔn)狀況下的HCl氣體6.72 L,若反應(yīng)過程中溶液的體積保持不變,則( )A. 反應(yīng)過程中得到6.72 L的氣體(標(biāo)況)B. 最終得到的溶液中c(Na)c(Cl)c(OH)C. 最終得到7.8 g的沉淀D. 最終得到的溶液中c(NaCl)0.1
25、5 mol/L*10. 已知在pH為4左右的環(huán)境中,Cu2、Fe2幾乎不水解,而Fe3幾乎完全水解。工業(yè)上制CuCl2是將濃鹽酸用蒸氣加熱到80左右,再慢慢加入粗氧化銅(含少量雜質(zhì)FeO),充分攪拌使之溶解。欲除去溶液中的雜質(zhì)離子,下述方法中可行的是( )A. 加入純Cu將Fe2還原為Fe B. 向溶液中通入H2S使Fe2沉淀C. 向溶液中通入Cl2,再通入NH3,調(diào)節(jié)pH為4左右D. 向溶液中通入Cl2,再加入純凈的CuO粉末調(diào)節(jié)pH為4左右11.將11.9 g Mg、Al、Fe組成的合金溶于足量的NaOH溶液中,合金質(zhì)量減少了2.7 g。另取等質(zhì)量的合金溶于過量稀硝酸中,生成了6.72 L
26、(標(biāo)準(zhǔn)狀況下)NO,向反應(yīng)后的溶液中加入適量NaOH溶液恰好使Mg2、Al3、Fe3完全轉(zhuǎn)化為沉淀,則沉淀的質(zhì)量為( )A. 22.1 g B. 27.2 g C. 30 g D. 無法確定12. 現(xiàn)有Al、Cl2、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六種物質(zhì),它們之間有如圖所示轉(zhuǎn)化關(guān)系,圖中每條線兩端的物質(zhì)之間都可以發(fā)生反應(yīng),下列推斷不合理的是( )A. N一定是HCl(aq) B. X可能為Al或Cl2C. Y一定為NaOH(aq) D. Q、Z中的一種必定為Al2O3二、非選擇題13. 根據(jù)下列框圖回答問題(答題時,方程式中的M、E用所對應(yīng)的元素符號表示):(1)
27、寫出M溶于H2SO4和H2O2混合液的化學(xué)方程式:_(2)某同學(xué)取X的溶液,酸化后加入淀粉KI溶液,變?yōu)樗{色。寫出與上述變化過程相關(guān)的離子方程式:_、_。(3)寫出N轉(zhuǎn)化為Z的現(xiàn)象及化學(xué)方程式:_。(4)寫出Cl2將Z氧化為K2EO4的化學(xué)方程式:_14. 聚合氯化鋁晶體的化學(xué)式為Al2(OH)nCl6n·xH2Om,它是一種高效無機水處理劑,它的制備原理是調(diào)節(jié)增大AlCl3溶液的pH,通過促進其水解而結(jié)晶析出。其制備原料主要是鋁加工行業(yè)的廢渣鋁灰,它主要含Al2O3、Al,還有SiO2等雜質(zhì)。聚合氯化鋁生產(chǎn)的工藝流程如下:(1)攪拌加熱操作過程中發(fā)生反應(yīng)的離子方程式:_
28、、_。(2)生產(chǎn)過程中操作B和D的名稱均為_(B和D為簡單操作)。(3)反應(yīng)中副產(chǎn)品a是_(用化學(xué)式表示)。(4)生產(chǎn)過程中可循環(huán)使用的物質(zhì)是_(用化學(xué)式表示)。(5)調(diào)節(jié)pH至4.04.5的目的是_。 (6)實驗室要測定水處理劑產(chǎn)品中n和x的值。為使測定結(jié)果更準(zhǔn)確,需得到的晶體較純凈。生產(chǎn)過程中C物質(zhì)可選用( )A. NaOH B. Al C. 氨水 D. Al2O3 E. NaAlO2*15.某化學(xué)興趣小組測定某FeCl3樣品(含少量FeCl2雜質(zhì))中鐵元素的質(zhì)量分數(shù),實驗時按以下步驟進行:稱量a g樣品,置于燒杯中 加入適量鹽酸和適量蒸餾水,使樣品溶解,然后準(zhǔn)確配制成250 mL溶液 準(zhǔn)
29、確量取25.00 mL步驟中配得的溶液,置于燒杯中,加入適量的氯水,加熱使反應(yīng)完全 趁熱迅速加入過量氨水,充分攪拌,使沉淀完全 過濾,洗滌沉淀 將沉淀轉(zhuǎn)移到坩堝內(nèi),加熱、攪拌,直到固體全部由紅褐色變?yōu)榧t棕色后,在干燥器中冷卻至室溫后,稱量 請根據(jù)上面的敘述,回答:(1)如圖所示儀器中,本實驗步驟中必須用到的儀器是E和_(填字母)。(2)寫出步驟中發(fā)生反應(yīng)的離子方程式_。(3)洗滌是洗去附著在沉淀上的_(寫離子符號),洗滌沉淀的操作是_。(4)第步操作中,將沉淀物加熱,冷卻至室溫,稱量其質(zhì)量為m1 g;再次加熱并冷卻至室溫,稱量其質(zhì)量為m2 g,且m1m20.3,接下來的操作應(yīng)當(dāng)是 _。(5)若
30、坩堝的質(zhì)量是W1,坩堝與加熱后固體的總質(zhì)量是W2,則樣品中鐵元素的質(zhì)量分數(shù)為_。(列出算式,無需化簡)(6)該興趣小組中的甲學(xué)生認為:實驗步驟中不加入氯水,其余步驟不變,仍可達到實驗?zāi)康摹D阏J為甲學(xué)生的觀點是否正確?_(填“正確”或“錯誤”),請說明理由:_。*16. 把由NaOH、AlCl3、MgCl2三種固體組成的混合物,溶于足量的水中,有0.58 g白色沉淀析出,向所得的溶液中,逐滴加入0.5 mol/L的鹽酸,加入鹽酸的體積和生成沉淀的質(zhì)量如圖所示。(1)混合物中NaOH的質(zhì)量是_g。(2)P點表示加入鹽酸的體積為_mL。17. 鐵是人體必需的微量元素,治療缺鐵性貧血的常見方法是服用補
31、鐵藥物。“速力菲”(主要成分:琥珀酸亞鐵,呈暗黃色)是一種市場上常見的補鐵藥物。該藥品不溶于水但能溶于人體中的胃酸。某同學(xué)為了檢測“速力菲”藥片中Fe2的存在,設(shè)計并進行了如下實驗:試回答下列問題:(1)試劑1是_,試劑2是_,加入新制氯水后溶液中發(fā)生的離子反應(yīng)方程式是 (2)加入試劑2后溶液的顏色由淡黃色轉(zhuǎn)變?yōu)榈t色是因為_ _ _,寫出2價Fe在空氣中轉(zhuǎn)化為3價Fe的化學(xué)方程式 (3)該同學(xué)猜想紅色溶液變?yōu)闊o色溶液的原因是溶液中的3價鐵被還原為2價鐵,你認為該同學(xué)的猜想合理嗎?_.若你認為合理,請說明理由(若你認為不合理,該空不作答)_;若你認為不合理,請?zhí)岢瞿愕牟孪氩⒃O(shè)計一個簡單的實驗加
32、以驗證(若你認為合理,該空不作答)_.1. D 解析:鋁是一種活潑的金屬,易與氧氣反應(yīng),但反應(yīng)后生成一層致密的氧化膜而阻止鋁與氧氣繼續(xù)反應(yīng),所以鋁具有較強的抗腐蝕性能。2. B 解析:中純鐵不易被銹蝕,中Fe位于第族,而不是B族,中當(dāng)鐵過量時可生成,可以通過化合反應(yīng)生成和,。3. A 解析:Mg、Al都可與稀H2SO4反應(yīng)放出H2,但遇濃H2SO4時Al在常溫下發(fā)生鈍化,Mg雖反應(yīng)但不產(chǎn)生H2。遇KOH只有Al反應(yīng)。與HNO3反應(yīng),HNO3為強氧化性酸,兩者都不會產(chǎn)生H2。4. A 解析:A項正確,因為Al粉能夠被NaOH溶液溶解,而Fe粉不能;B項瓷坩堝中SiO2與NaOH反應(yīng);C項Fe(O
33、H)3固體不溶于水。方法:把少量FeCl3飽和溶液逐滴滴入沸水中再煮沸至呈紅褐色,F(xiàn)eCl33H2O(沸水)Fe(OH)3(膠體)3HCl;D項HCO、HSO、SO都能與鹽酸反應(yīng)放出CO2或SO2與澄清石灰水反應(yīng)產(chǎn)生沉淀。5. C 解析:鋁在常溫下與空氣中的氧氣反應(yīng),在鋁表面形成一層致密的氧化物薄膜;鋁與氯氣反應(yīng)生成氯化鋁;氧化鋁是兩性氧化物,既能與酸反應(yīng),也能與堿反應(yīng)。*6. B解析:由b<c可知一定有Cu生成,而Fe粉可能不足,也可能過量,即溶液中一定有Fe2,一定無Fe3,可能有Cu2,殘余固體可能為Cu,也可能為Cu、Fe的混合物。7. C解析:A項,BaCO3、BaSO3都與H
34、反應(yīng),不可能存在于強酸性環(huán)境中;B項,加Cu(NO3)2固體后會發(fā)生:3Cu8H2NO3Cu22NO4H2O的離子反應(yīng),銅粉會溶解;C項,發(fā)生的反應(yīng)依次為:Al33NH3·H2OAl(OH)33NH,Al(OH)33HAl33H2O;D項,ZnCu2Zn2Cu,生成的少量Cu附著在Zn粒上,形成CuZn原電池,會加速產(chǎn)生H2的速率。*8. B 解析:由反應(yīng)過程可知,Z與KSCN溶液反應(yīng)后溶液顯血紅色,Z中一定有Fe3;而X中不一定有Fe3,也可能是Fe2被硝酸根氧化為Fe3,AgI沉淀為黃色而不是淺黃色,AgBr為淺黃色沉淀,所以只有B項正確。*9. C 解析:由題n(Na2O2)0
35、.2 mol,n(Al)0.2 mol,可知發(fā)生反應(yīng):2Na2O22H2O4NaOHO2,2Al2NaOH2H2O2NaAlO23H2,可知生成氣體0.4 mol,標(biāo)況下體積為8.96 L;加入鹽酸先和過量的NaOH反應(yīng),剩余0.1 mol和NaAlO2反應(yīng)生成0.1 mol Al(OH)3:NaAlO2HClH2ONaClAl(OH)3,最終溶液為0.3 mol NaCl、0.1 mol NaAlO2。*10. D 解析:本題考查學(xué)生對水解知識的應(yīng)用,同時也考查學(xué)生對除雜質(zhì)方法的了解程度。所得溶液中的雜質(zhì)離子為Fe2。向溶液中通入Cl22Fe2Cl22Fe32Cl。加入純凈的CuO粉末調(diào)節(jié)p
36、H為4左右,F(xiàn)e3幾乎完全水解,過濾,除去Fe(OH)3和多余的CuO粉末。11. B 解析:已知鋁為2.7 g即0.1 mol,因1 mol Mg、1 mol Fe、1 mol Al與過量稀硝酸反應(yīng)時可得到2/3 mol NO、1 mol NO、1 mol NO,設(shè)鎂、鐵的物質(zhì)的量分別為x、y,24x56y9.2 g,2/3xy0.1 mol0.2 mol,解得x0.15 mol,y0.1 mol。得到的沉淀為0.15 mol Mg(OH)2、0.1 mol Fe(OH)3、0.1 mol Al(OH)3的混合物,故答案為B。12. B 解析:在Al、Cl2、Al2O3、HCl(aq)、Al
37、(OH)3、NaOH(aq)中,只有NaOH(aq)能與Al、Cl2、Al2O3、HCl(aq)、Al(OH)3五種物質(zhì)反應(yīng),對照轉(zhuǎn)化關(guān)系圖,可知Y為NaOH(aq)。只有HCl(aq)能與Al、Al2O3、Al(OH)3、NaOH(aq)四種物質(zhì)反應(yīng),對照圖示轉(zhuǎn)化關(guān)系可知N為HCl(aq),故選項A、C正確。選項B,若X為Al,Al能與Cl2、HCl(aq)、NaOH(aq)三種物質(zhì)反應(yīng),而圖示給出的是與兩種物質(zhì)反應(yīng),所以X不可能是Al,但可能是Cl2。選項D,Al2O3既能與HCl(aq)反應(yīng),也能與NaOH(aq)反應(yīng),故Q、Z中的一種必定為Al2O3。13. (1)CuH2O2H2SO
38、4CuSO42H2O(2)4Fe2O24H4Fe32H2O 2Fe32I2Fe2I2(3)白色沉淀迅速轉(zhuǎn)化為灰綠色,最后變?yōu)榧t褐色,4Fe(OH)2O22H2O4Fe(OH)3(4)10KOH3Cl22Fe(OH)32K2FeO46KCl8H2O解析:分析本題應(yīng)從M為紅色金屬(Cu)和Y與KSCN溶液反應(yīng)變紅色著手。從轉(zhuǎn)化圖中的轉(zhuǎn)化關(guān)系和現(xiàn)象可知,E、X、Y、N、Z、K2EO4中均含有鐵元素,且Y含F(xiàn)e3,則Z為Fe(OH)3,N為Fe(OH)2,X為FeSO4,E為Fe。確定好相關(guān)物質(zhì)后,即可完成各問題。14. (1)Al2O36H2Al33H2O 2Al6H2Al33H2(2)過濾 (3)
39、H2 (4)HCl (5)促進AlCl3水解,使晶體析出 (6)BD解析:由于鋁灰中含Al2O3、Al,還有SiO2等雜質(zhì),加入鹽酸攪拌使Al元素進入溶液,發(fā)生反應(yīng)Al2O36H2Al33H2O,2Al6H2Al33H2,和SiO2等雜質(zhì)分離。采取過濾的方法得到AlCl3溶液,溶液降溫熟化調(diào)節(jié)pH至4.04.5,增大AlCl3溶液的pH,通過促進其水解而結(jié)晶析出。AlCl3水解生成的HCl易揮發(fā),揮發(fā)出的HCl經(jīng)水噴淋吸收又生成鹽酸這個過程中可以循環(huán)利用鹽酸。為了不引進新的雜質(zhì),可以選擇B和D。*15. (1)CFG (2)2Fe2Cl22Fe32Cl (3)NH、Cl、OH 向漏斗里注入蒸餾水,使水面沒過濾渣,水自然流完后,重復(fù)操作23次 (4)繼續(xù)加熱,放置于干燥器中冷卻,稱量,至最后兩次稱得的質(zhì)量差不超過0.1 g為止(5)×100%(6)正確 FeCl3、FeCl2溶液中加入過量氨水
溫馨提示
- 1. 本站所有資源如無特殊說明,都需要本地電腦安裝OFFICE2007和PDF閱讀器。圖紙軟件為CAD,CAXA,PROE,UG,SolidWorks等.壓縮文件請下載最新的WinRAR軟件解壓。
- 2. 本站的文檔不包含任何第三方提供的附件圖紙等,如果需要附件,請聯(lián)系上傳者。文件的所有權(quán)益歸上傳用戶所有。
- 3. 本站RAR壓縮包中若帶圖紙,網(wǎng)頁內(nèi)容里面會有圖紙預(yù)覽,若沒有圖紙預(yù)覽就沒有圖紙。
- 4. 未經(jīng)權(quán)益所有人同意不得將文件中的內(nèi)容挪作商業(yè)或盈利用途。
- 5. 人人文庫網(wǎng)僅提供信息存儲空間,僅對用戶上傳內(nèi)容的表現(xiàn)方式做保護處理,對用戶上傳分享的文檔內(nèi)容本身不做任何修改或編輯,并不能對任何下載內(nèi)容負責(zé)。
- 6. 下載文件中如有侵權(quán)或不適當(dāng)內(nèi)容,請與我們聯(lián)系,我們立即糾正。
- 7. 本站不保證下載資源的準(zhǔn)確性、安全性和完整性, 同時也不承擔(dān)用戶因使用這些下載資源對自己和他人造成任何形式的傷害或損失。
最新文檔
- 物理高考題及答案打印
- 安徽醫(yī)科大學(xué)臨床醫(yī)學(xué)院《工程數(shù)學(xué)A》2023-2024學(xué)年第一學(xué)期期末試卷
- 天津市2025屆三年級數(shù)學(xué)第二學(xué)期期末調(diào)研試題含解析
- 遂寧市重點中學(xué)2024-2025學(xué)年高三最后一考歷史試題試卷含解析
- 天津師范大學(xué)津沽學(xué)院《社會化營銷案例研究》2023-2024學(xué)年第二學(xué)期期末試卷
- 2025屆貴州省凱里一中等重點中學(xué)高三下學(xué)期4月綜合測試(二)語文試題含解析
- 永州職業(yè)技術(shù)學(xué)院《歷代名著導(dǎo)讀》2023-2024學(xué)年第二學(xué)期期末試卷
- 安徽省馬鞍山市和縣一中2024-2025學(xué)年高三年級元月調(diào)研考試語文試題含解析
- 浙江省紹興市越城區(qū)2024-2025學(xué)年三年級數(shù)學(xué)第二學(xué)期期末統(tǒng)考模擬試題含解析
- 貴州電子科技職業(yè)學(xué)院《外國歷史要籍介紹》2023-2024學(xué)年第二學(xué)期期末試卷
- 人教部編本八年級語文上冊第六單元復(fù)習(xí)課件共26張
- 騰訊社招測評題庫
- 家鄉(xiāng)二聲部合唱譜
- 2023年公共營養(yǎng)師之三級營養(yǎng)師全國通用試題
- 《無人機概論》第1章 無人機概述
- 售后工程師的數(shù)據(jù)分析能力
- 鞋業(yè)成本分析與控制
- 典當(dāng)行行業(yè)報告
- 食品新產(chǎn)品開發(fā) 課件 第三章 食品新產(chǎn)品開發(fā)配方設(shè)計
- 《幼兒園課程》第1章:幼兒園課程概述
- 診所消防安全培訓(xùn)課件

評論
0/150
提交評論