



版權(quán)說明:本文檔由用戶提供并上傳,收益歸屬內(nèi)容提供方,若內(nèi)容存在侵權(quán),請進行舉報或認領(lǐng)
文檔簡介
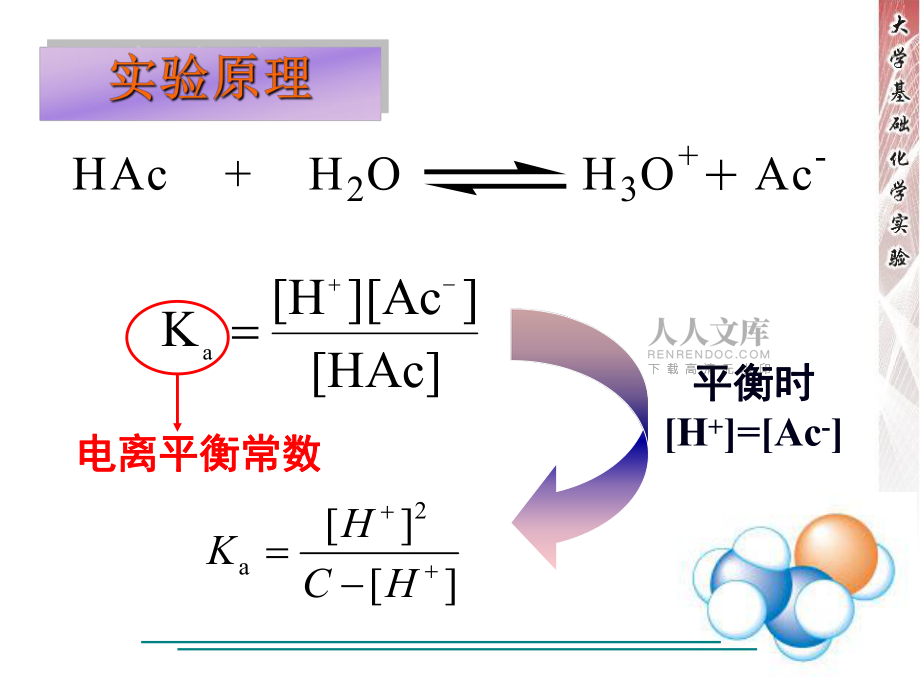
1、HAc + H2OH3O+ Ac-+ HAcAcHKa電離平衡常數(shù)電離平衡常數(shù)2aHCHK平衡時平衡時H+=Ac-%(100解質(zhì)之和)已電離的和未電離的電已電離的電解質(zhì))nn電離度電離度CH5%CHK2a2aHCHK當(dāng)當(dāng)5%5%時時(表示弱電解質(zhì)在溶液中的電離程度)(表示弱電解質(zhì)在溶液中的電離程度)物質(zhì)的量物質(zhì)的量PHS-3型酸度計的組成示意圖型酸度計的組成示意圖選擇定位斜率溫度酸度計的面板示意圖酸度計的面板示意圖H HF F2.303RT2.303RTE EE Ep E參比池 R Re ed d O Ox x l ln nn nF FR RT TE EE ENernst方程方程:H HF F
2、2 2. .3 30 03 3R RT TE EE Ep指示H HF F2.303RT2.303RTpA(A為常數(shù)為常數(shù))A為常數(shù)時為常數(shù)時,原電池的電動勢與溶液的原電池的電動勢與溶液的pH具具有直線關(guān)系有直線關(guān)系,該直線的斜率為該直線的斜率為2.303RT/F氧化態(tài)氧化態(tài)還原態(tài)還原態(tài)參比電極:甘汞電極參比電極:甘汞電極指示電極:玻璃電極指示電極:玻璃電極復(fù)合電極復(fù)合電極指示電極和參比電極同時浸入試液中構(gòu)成一指示電極和參比電極同時浸入試液中構(gòu)成一個原電池時,通過測定原電池的電動勢,即個原電池時,通過測定原電池的電動勢,即可求得被測離子的活度可求得被測離子的活度( (或濃度或濃度) )。標定分為
3、單點標定或兩點標定標定分為單點標定或兩點標定預(yù)熱的目的是什么?預(yù)熱的目的是什么?單點標定:一般測量單點標定:一般測量兩點標定:高精度的測量兩點標定:高精度的測量測量:溶液濃度均勻,讀取穩(wěn)定的數(shù)值測量:溶液濃度均勻,讀取穩(wěn)定的數(shù)值洗凈洗凈水除去水除去用待測液用待測液潤洗潤洗三次三次取液取液放液放液(左手拿接受容器并傾斜左手拿接受容器并傾斜,使內(nèi)壁緊使內(nèi)壁緊貼移液管尖貼移液管尖, 移液管垂直,松開右手食移液管垂直,松開右手食指指, 使溶液自由地沿壁流下。使溶液自由地沿壁流下。)定量定量(視線視線平視時彎月面與標線相切時平視時彎月面與標線相切時,立即按緊食指立即按緊食指)查漏查漏洗滌洗滌定量定量溶液混勻溶液混勻定量定量轉(zhuǎn)移時,燒杯口應(yīng)緊靠伸入容量瓶的轉(zhuǎn)移時,燒杯口應(yīng)緊靠伸入容量瓶的攪拌棒(攪拌棒(其上部不要碰瓶口,下端靠著瓶其上部不要碰瓶口,下端靠著瓶頸內(nèi)壁頸內(nèi)壁),使溶液沿攪拌捧和內(nèi)壁流入。),使溶液沿攪拌捧和內(nèi)壁流入。溶液全部轉(zhuǎn)移后,用洗瓶吹溶液全部轉(zhuǎn)移后,用洗瓶吹洗攪棒和燒杯洗攪棒和燒杯內(nèi)壁多次并全部轉(zhuǎn)移。當(dāng)加水至容量瓶的內(nèi)壁多次并全部轉(zhuǎn)移。當(dāng)加水至容量瓶的四分之三左右時,用右手食指和中指夾住四分之三左右時,用右手食指和中指夾住2.50mL5.00mL25.00mL已知濃度的已知濃度的HAc于三個于三個50mL容量瓶
溫馨提示
- 1. 本站所有資源如無特殊說明,都需要本地電腦安裝OFFICE2007和PDF閱讀器。圖紙軟件為CAD,CAXA,PROE,UG,SolidWorks等.壓縮文件請下載最新的WinRAR軟件解壓。
- 2. 本站的文檔不包含任何第三方提供的附件圖紙等,如果需要附件,請聯(lián)系上傳者。文件的所有權(quán)益歸上傳用戶所有。
- 3. 本站RAR壓縮包中若帶圖紙,網(wǎng)頁內(nèi)容里面會有圖紙預(yù)覽,若沒有圖紙預(yù)覽就沒有圖紙。
- 4. 未經(jīng)權(quán)益所有人同意不得將文件中的內(nèi)容挪作商業(yè)或盈利用途。
- 5. 人人文庫網(wǎng)僅提供信息存儲空間,僅對用戶上傳內(nèi)容的表現(xiàn)方式做保護處理,對用戶上傳分享的文檔內(nèi)容本身不做任何修改或編輯,并不能對任何下載內(nèi)容負責(zé)。
- 6. 下載文件中如有侵權(quán)或不適當(dāng)內(nèi)容,請與我們聯(lián)系,我們立即糾正。
- 7. 本站不保證下載資源的準確性、安全性和完整性, 同時也不承擔(dān)用戶因使用這些下載資源對自己和他人造成任何形式的傷害或損失。
最新文檔
- 鍛鑄鋼件行業(yè)深度研究分析報告(2024-2030版)
- 2025年腳踏單雙氣筒項目投資可行性研究分析報告
- 中國2-氟吡啶項目投資計劃書
- 企業(yè)信用報告-浙江瑞天建設(shè)有限公司
- 中國電動彎排機行業(yè)市場前景預(yù)測及投資價值評估分析報告
- 商業(yè)計劃書范例
- 中國垃圾處理環(huán)保設(shè)備行業(yè)市場前景預(yù)測及投資價值評估分析報告
- 鉿科(北京)控股有限公司介紹企業(yè)發(fā)展分析報告
- 建筑結(jié)構(gòu)膠項目投資可行性研究分析報告(2024-2030版)
- 2025年中國泥炭土項目創(chuàng)業(yè)計劃書
- 知識圖譜構(gòu)建與應(yīng)用試題及答案
- 湖北省武漢市2025屆高三五月模擬訓(xùn)練英語試題(含答案無聽力原文及音頻)
- 基因編輯技術(shù)的臨床應(yīng)用與未來發(fā)展方向-洞察闡釋
- 靜脈輸液不良反應(yīng)應(yīng)急預(yù)案與處理流程
- 《論亞太局勢》課件
- 基于深度學(xué)習(xí)的日志異常檢測技術(shù)研究
- 大學(xué)生勞動就業(yè)法律問題解讀(華東理工大學(xué))智慧樹知到見面課、章節(jié)測試、期末考試答案
- 水電站收購分析報告
- 水泥粉助磨劑項目可行性研究報告發(fā)改委立項模板
- 濟南公共交通集團有限公司招聘筆試題庫2025
- 工貿(mào)行業(yè)重大安全生產(chǎn)事故隱患判定標準解讀課件

評論
0/150
提交評論