



版權(quán)說明:本文檔由用戶提供并上傳,收益歸屬內(nèi)容提供方,若內(nèi)容存在侵權(quán),請進(jìn)行舉報或認(rèn)領(lǐng)
文檔簡介
1、高二化學(xué)下學(xué)期月考試卷可能用到的相對原子質(zhì)量:H-l C-12 N-14 0-16 Mg24 Al27 S-32 Cl-35.5 Fe-56 Cu64一、單項選擇題1 .綠色化學(xué)的核心確實是利用化學(xué)原理從源頭上減少和排除工業(yè)生產(chǎn)對環(huán)境的污染。下列做法不符合綠 色化學(xué)理念的是A.研制水溶劑涂料替代有機溶劑涂料B.用可降解塑料生產(chǎn)包裝盒或快餐盒C.用反應(yīng):Cu +2H2SO4 ()-CuSO4+SO2 t +2H2O 制備硫酸銅D.用反應(yīng):2cH2=CH2+O2->2cK>h制備環(huán)氧乙烷2 .下列有關(guān)物質(zhì)分類或歸類正確的是混合物:石炭酸、福爾馬林、水玻璃、水銀化合物:CaCL、燒堿、聚
2、苯乙烯、HD 電解質(zhì):硫酸、膽磯、冰醋酸、硫酸鋼 同系物:CHM、GHQ:、CKO:、CH。同素異形體:Go、C:。、金剛石、石墨A. ©© B. ®® C.®© D.3 .下列有關(guān)化學(xué)用語正確的是A.乙醇、乙二醇、丙三醇互為同系物,同系物之間不可能為同分異物體B.北京奧運會獎牌“金鑲玉”獎牌玉的化學(xué)成分多為含水鈣鎂硅酸鹽,如:Ca2Mg5SisO22(OH)2 可用氧化物表示為:2CaO 5MgO 8SiO2 H20C.次氯酸的結(jié)構(gòu)式為:HC0鬟.D.丙烷分子的比例模型示意圖:V*4 .用一張已除去表面氧化膜的鋁箔緊緊包裹在試管外壁
3、(如右圖),將試管浸入硝酸汞溶液中,片刻取出, 然后置于空氣中,不久鋁箔表而生出“白毛”,紅墨水柱右端上升。依照實驗現(xiàn)象判定下列說法錯誤的 是HA.鋁是一種較爽朗的金屬,%B.鋁與氧氣反應(yīng)放出大量的熱量整(JC.鋁片上生成的白毛是氧化鋁和氧化汞的混合物甯D.實驗中發(fā)生的反應(yīng)差不多上氧化還原反應(yīng)5 .下列各溶液中,各離子可能大量共存的有A.含有大量 Ba?+的溶液中:HCO3 Fe3+、Ag+、SO/-、SCNB.由水電離的 c(OH )=10-,4mol L_,的溶液中:CH3coO、C6HsO Na K+C.滴加無色酚醐試液后仍無色的溶液中:Na+、832, K+、CIO A1O2-D.加入
4、鋁粉后產(chǎn)生氫氣的溶液中:NH-、Na NO3, CW S26 . CIO2是一種消毒殺菌效率高、二次污染小的水處理劑。實驗室能夠通過以下反應(yīng)制得CIO”2KCIO3 + H2C2O4 + H2SO4 = 2C1O21 + K2SO4 + 2CO2 t + 2H2O下列說法正確的是A. KQO3在反應(yīng)中得到電子B. C1O2是氧化產(chǎn)物C.H2c2O4在反應(yīng)中被還原D.1 mol KCKh參加反應(yīng)有2 mol電子轉(zhuǎn)移7 .已知在粗碘中含IC1和IBr,受熱時IC1、IBr均可升華;若在粗碘中加入一種物質(zhì)再進(jìn)行升華,則可 制得精碘。在下列物質(zhì)中,應(yīng)加入的物質(zhì)是A. H:0B. ZnC. KID. N
5、aCl8 .玻璃棒是化學(xué)實驗中常用的儀器,其作用是用于攪拌、過濾或轉(zhuǎn)移液體時引流。下列有關(guān)實驗過程中, 一樣不需要使用玻璃棒進(jìn)行操作的是 用pH試紙測定Na2c。3溶液的pH從氯酸鉀和二氧化鎰制取氧氣的剩余固體中提取KC1實驗室用新制的FeSO«溶液和預(yù)處理過的NaOH溶液制備Fe(OH)2白色沉淀用已知濃度的鹽酸和未知濃度的氫氧化鈉溶液進(jìn)行中和滴定實驗將適量氯化鐵飽和溶液滴入沸水中制氫氧化鐵膠體用適量的蔗糖、濃硫酸和水在小燒杯中進(jìn)行濃硫酸的脫水性實驗探究Ba(OH)2.8H2O晶體和NH4C1晶體反應(yīng)過程中的能量變化A. ©© B.©C. ©
6、©D. ©©二、不定項選擇題9.下列離子方程式書寫正確的是A.過氧化鈉固體與水反應(yīng):201 +2H2O = 40H +02 tB. NaHS 溶液呈堿性:HS-+ H3O+ # H2S + H2OC. 4moi/L的KAI (S04) 2溶液與7 moi/L的Ba (OH) 2溶液等體積混合:4Al3*+7SO42-+7Ba2+14OH-=2Al (OH) 3I+2AIO廠+7BaSO41+4HqD.稀 HNO3 中加入過量鐵粉:Fe + NO3 + 4H+ = Fe3+ + NO t + 2H2O10.某二元酸(H?A)按下式發(fā)生電離:H2A = H+HA ;
7、HA = FT+A?,現(xiàn)有下列四種溶液:0.01 mol L1的H2A溶液 O.Olmol L 1 NaHA 溶液0.02n】ol L1的HC1溶液與0.04mol L1的NaHA溶液等體積混合0.02mol L 1的NaOH溶液與0.02mol - L 的NaHA溶液等體積混合下列關(guān)于上述四種溶液的說法正確的是A.溶液中存在水解平穩(wěn):HA +H2O OH2A+OHB.溶液中有:c(HA )+2c(A2 )=c(Na+)C.溶液中有:c(OH )=c(H+)+c(HA-)D.四種溶液中c(HA )濃度大小:下 11.依照下列實驗現(xiàn)象,所得結(jié)論正確的是ABCD實驗實驗現(xiàn)象結(jié)論A左燒杯中鐵表而有氣
8、泡,右邊燒杯中銅表面有氣泡活動性:Al>Fe>CuB左邊棉花變?yōu)槌壬疫吤藁ㄗ優(yōu)樗{(lán)色氧化性:Cl2>Br2>l2C白色固體先變?yōu)榈S色,后變?yōu)楹谏芙舛龋篈gCl>AgBr>Ag2SD錐形瓶中有氣體產(chǎn)生,燒杯中液體變渾濁非金屬性:CI>C>Si12 .有一種鋰電池,它是用金屬鋰和石墨作電極材料,電解質(zhì)溶液是由LiAlCL溶解在亞硫酰氯(SOCL) 中形成的,電池總反應(yīng)方程式為:8Li +3S0Cl:=6LiCl +Li:S03 +2S,下列有關(guān)敘述正確的是A.金屬鋰作電池的正極,石墨作電池的負(fù)極B.電池工作過程中,SOCL被還原為Li:SO,C
9、.電解質(zhì)溶液中混入水,對電池反應(yīng)無阻礙D.電池工作過程中,金屬鋰提供的電子與正極區(qū)析出硫的物質(zhì)的量之比為4 : 113 .化合物A經(jīng)李比希法和質(zhì)譜法分析得知其相對分子質(zhì)量為136,分子式C8H式)” A分子中只含一個苯 環(huán)且苯環(huán)上只有一個取代基,其核磁共振氫譜與紅外光譜如圖。關(guān)于A的下列說法中,不正確的是A. A分子屬于酯類化合物,在一定條件下能發(fā)生水解反應(yīng)B. A在一定條件下可與4 moi H?發(fā)生加成反應(yīng)C.符合題中A分子結(jié)構(gòu)特點的有機物只有一種D.與A屬于同類化合物的同分異構(gòu)體只有2種14.在一定溫度條件下,甲、乙兩個容積相等的恒容密閉容器中均發(fā)生如下反應(yīng): 3A(g)+B(g),vC(
10、g)+D(s),向甲中通入 6molA 和 2moiB,向乙中通入 1.5molA、0.5molB 和 3moic 和2molD,反應(yīng)一段時刻后都達(dá)到平穩(wěn),現(xiàn)在測得甲、乙兩容器中C的體枳分?jǐn)?shù)都為0.2,下列敘述 中正確的是A.平穩(wěn)時,甲、乙兩容器中A、B的物質(zhì)的量之比不相等B.若平穩(wěn)時,甲、乙兩容器中A的物質(zhì)的量相等,則x=2C.平穩(wěn)時甲中A的體積分?jǐn)?shù)為40%D.若平穩(wěn)時兩容器中的壓強不相等,則兩容器中壓強之比為5 : 8三、(本題包括1小題)15. DIS數(shù)字化信息系統(tǒng)因為能夠準(zhǔn)確測量溶液的pH而在中和滴定的研究中應(yīng)用越來越廣泛深入。某學(xué) 習(xí)小組利用DIS系統(tǒng)探究強堿和不同酸的中和反應(yīng)的過程
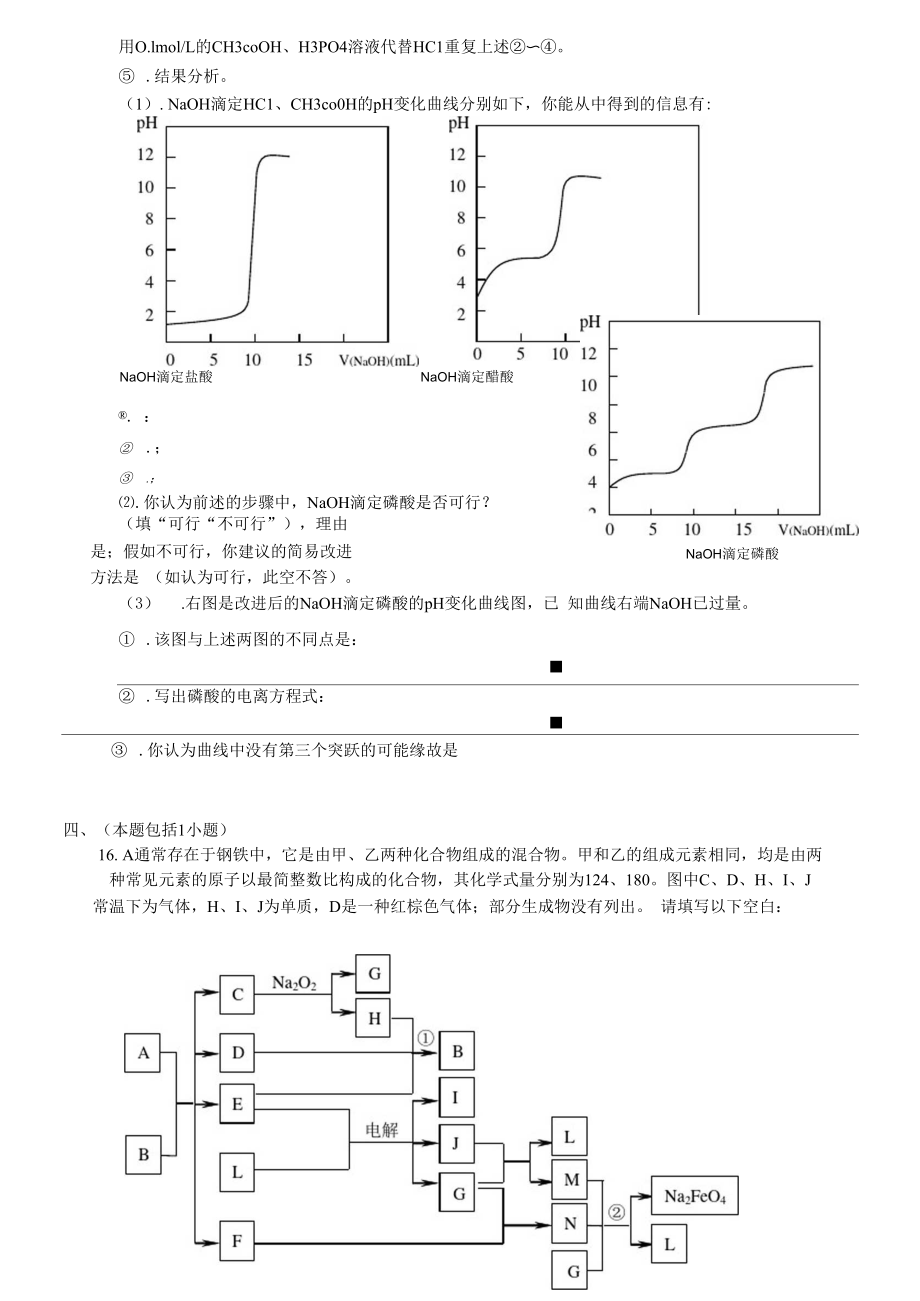
11、如下:實驗步驟: .分別配制 O.lmol/L 的 NaOH、HCR CH3coOH、H3PO4溶液備用。 .在錐形瓶中加入lOmLO.lmol/L的HC1,在25.00mL堿式滴定管中加入O.lmol/L的NaOH,連 接數(shù)據(jù)采集器和pH傳感器。 .向錐形瓶中滴入NaOH,接近估算的NaOH用量鄰近時,減慢滴加速度,等讀數(shù)穩(wěn)固后,再滴 下一滴NaOHo .儲備運算機繪制的pH變化圖。用O.lmol/L的CH3coOH、H3PO4溶液代替HC1重復(fù)上述。 .結(jié)果分析。(1). NaOH滴定HC1、CH3co0H的pH變化曲線分別如下,你能從中得到的信息有:NaOH滴定磷酸NaOH滴定鹽酸NaO
12、H滴定醋酸®. : .; .;.你認(rèn)為前述的步驟中,NaOH滴定磷酸是否可行? (填“可行“不可行”),理由是;假如不可行,你建議的簡易改進(jìn)方法是 (如認(rèn)為可行,此空不答)。(3) .右圖是改進(jìn)后的NaOH滴定磷酸的pH變化曲線圖,已 知曲線右端NaOH已過量。 .該圖與上述兩圖的不同點是: .寫出磷酸的電離方程式: .你認(rèn)為曲線中沒有第三個突躍的可能緣故是四、(本題包括1小題)16. A通常存在于鋼鐵中,它是由甲、乙兩種化合物組成的混合物。甲和乙的組成元素相同,均是由兩種常見元素的原子以最簡整數(shù)比構(gòu)成的化合物,其化學(xué)式量分別為124、180。圖中C、D、H、I、J常溫下為氣體,H、
13、I、J為單質(zhì),D是一種紅棕色氣體;部分生成物沒有列出。 請?zhí)顚懸韵驴瞻祝海?)C的電子式為,甲和乙的化學(xué)式分別為、:(2)反應(yīng)的化學(xué)方程式;電解E、L混合物的離子方程式:(3)鋼鐵的表面發(fā)藍(lán)、發(fā)黑處理是常用的防腐方法。6Na2FeO2+ NaNO2+ 5H2O = 6NaFeO2+ NH3 t + 7NaOH是要緊處理反應(yīng)之一。而工業(yè)上一樣不用冷濃硝酸進(jìn)行鐵表而處理,其可能的緣故 是:。五、(本題包括1小題)17 .目前用于抗幽門螺旋桿菌的常見高效抗生素是氨茉青鞋素,它可由青霉素來合成。青霉素(G6H18N2O4S)氨葦青霉素(Cl6H19N3O4S)O0 II一定條件II已知:一C-NH 十
14、HQ-C-OH+H.N-請回答下列問題:寫出反應(yīng)的反應(yīng)類型, , , 寫出D的結(jié)構(gòu)簡式寫出反應(yīng)的化學(xué)方程式:六、(本題包括1小題)18 .“嫦娥一號”登月成功,實現(xiàn)了中國人“奔月”的妄圖。(1) “嫦娥一號”使用的推進(jìn)劑是液氫和液氧,這種推進(jìn)劑的優(yōu)點是:,(請寫兩條)(2)下列是298K時,氫氣(比)、碳(C)、辛烷(GH|8)、甲烷(CH4)燃燒的熱學(xué)化方程式:H2 (g) +l/2O2 (g) H20 (1): AH=-285.8kJ/molC (g) +O2 (g) C02 一 (g); AH=-393.5kJ/molCSH1S (1) +25/20? (g) 8CO2 (g) +9H2
15、O (1); AH=-5518kJ/molCH4 (g) +2O2 (g) C02 (g) +2H2O (1): AH=-890.3kJ/mol相同質(zhì)量的H2、C、CsH18、CH完全燃燒時,放出熱量最多的是,通過運算說明等質(zhì) 量的氫氣和碳燃燒時產(chǎn)生熱量的比是(保留1位小數(shù))。 (3)已知:H2 (g) =H2 (I): AH=-0.92kJ/mol O2 (g) O2 (1): AH=-6.84kJ/molH20 (1) =H20 (g); AH=+44.0kJ/mol請寫出液氫和液氧生成氣態(tài)水的熱化學(xué)方程式:假如此次嫦娥一號所攜帶的燃料為45噸,液氫、液氧恰好完全反應(yīng)生成氣態(tài)水,總共開釋能
16、量 kJ (保留3位有效數(shù)字)。(4)氫氣、氧氣不僅燃燒時能開釋熱能,二者形成的原電池還能提供電能,美國的探月飛船“阿波羅 號”使用的確實是氫氧燃料電池,電解液為KOH溶液,其電池反應(yīng)式為:負(fù) 極:: 正極::總反應(yīng)式:(5)若用氫氧燃料電池電解由NaCl和CuSCU組成的混合溶液,其中c (Na+) =3c (Cu2+) =0.3mol LI取該混合液100mL用石墨做電極進(jìn)行電解,通電一段時刻后,在陰極收集到0.U2L (標(biāo)準(zhǔn)狀 況)氣體。(寫出運算過程)若溶液體積仍為100mL,現(xiàn)在溶液的pH為多少?(不考慮硫酸銅水解)現(xiàn)在氫氧燃料電池中消耗Hz和的質(zhì)量各是多少?(保留2位小數(shù))七、(本
17、題包括1小題)19.元素周期表中第四周期元素由于受3d電子的阻礙,性質(zhì)的遞變規(guī)律與短周期元素略有不同。(1)第四周期過渡元素的明顯特點是形成多種多樣的配合物。CO能夠和專門多過渡金屬形成配合物,如城基鐵Fe(CO)J、撥基鍥Ni(CO)4o CO分子中C 原子上有一對孤對電子,C、O原子都符合8電子穩(wěn)固結(jié)構(gòu),CO的結(jié)構(gòu)式為,與 CO互為等電子體的二價陰離子為 (填電子式)。 金屬銀粉在CO氣流中輕微加熱,生成液態(tài)Ni(CO)4分子。423K時,Ni(CO)4分解為Ni和CO,從 而制得高純度的Ni粉。試估量Ni(COL易溶于下列 0水 b.四氯化碳 c.苯 d.硫酸銀溶液(2)第四周期元素的第
18、一電離能隨原子序數(shù)的增大,總趨勢是逐步增大的。錢的基態(tài)原子的電子排布式是, Ga的第一電離能卻明顯低于Zn,緣故是 0<3)用價層電子對互斥理論推測H£e和BBd的立體結(jié)構(gòu),兩個結(jié)論都正確的是a.直線形;三角錐形6.V形:三角錐形。.直線形;平而三角形d.V形:平而三角形化學(xué)參考答案1. C 2. D 3. B 4. C 5. B 6. A 7. C 8. B9. C 10, CD 11 AC 12. D 13. BD 14. B三、(本題包括1小題,)答案起點pH不同,鹽酸的小,醋酸的大:均有一個pH突躍;鹽酸中開始pH上升慢,突躍 前突然變快,醋酸中開始pH上升快,突躍前因為緩沖溶液的作用而使pH上升變慢。不可行;NaOH的用量超過了所用堿式滴定管的最大體積讀數(shù):減少磷酸的體枳:有兩個pH突躍;H+ + H2PO4: H2PO4 H+ + HPO: : HPO: 、H+ + PO,NaHPO的堿性差不多較強,pH較大,與NaOH反應(yīng)生成Na3P04后,pH變化不大,因此沒有pH 突躍現(xiàn)象。四、(本題包括1小題)16 . (1) o:C:0 Fe2c Fe3c(2 ) 4NO2+O2+2H2O=4HNO32C1+ 2Hg二電二 2OH + H2T + Ch?(3)硝酸易揮發(fā),且不穩(wěn)固,見光易分解,故不易操作;生成物對環(huán)境污染嚴(yán)峻五
溫馨提示
- 1. 本站所有資源如無特殊說明,都需要本地電腦安裝OFFICE2007和PDF閱讀器。圖紙軟件為CAD,CAXA,PROE,UG,SolidWorks等.壓縮文件請下載最新的WinRAR軟件解壓。
- 2. 本站的文檔不包含任何第三方提供的附件圖紙等,如果需要附件,請聯(lián)系上傳者。文件的所有權(quán)益歸上傳用戶所有。
- 3. 本站RAR壓縮包中若帶圖紙,網(wǎng)頁內(nèi)容里面會有圖紙預(yù)覽,若沒有圖紙預(yù)覽就沒有圖紙。
- 4. 未經(jīng)權(quán)益所有人同意不得將文件中的內(nèi)容挪作商業(yè)或盈利用途。
- 5. 人人文庫網(wǎng)僅提供信息存儲空間,僅對用戶上傳內(nèi)容的表現(xiàn)方式做保護(hù)處理,對用戶上傳分享的文檔內(nèi)容本身不做任何修改或編輯,并不能對任何下載內(nèi)容負(fù)責(zé)。
- 6. 下載文件中如有侵權(quán)或不適當(dāng)內(nèi)容,請與我們聯(lián)系,我們立即糾正。
- 7. 本站不保證下載資源的準(zhǔn)確性、安全性和完整性, 同時也不承擔(dān)用戶因使用這些下載資源對自己和他人造成任何形式的傷害或損失。
最新文檔
- 南京中醫(yī)藥大學(xué)翰林學(xué)院《定性數(shù)據(jù)分析》2023-2024學(xué)年第二學(xué)期期末試卷
- 山東工藝美術(shù)學(xué)院《操作系統(tǒng)原理實驗課》2023-2024學(xué)年第二學(xué)期期末試卷
- 九江學(xué)院《民舞-運動舞蹈劇目排練與實踐》2023-2024學(xué)年第二學(xué)期期末試卷
- 山東省淄博市臨淄區(qū)2024-2025學(xué)年三年級數(shù)學(xué)第二學(xué)期期末聯(lián)考模擬試題含解析
- 綿陽城市學(xué)院《醫(yī)學(xué)影像成像原理》2023-2024學(xué)年第二學(xué)期期末試卷
- 四川護(hù)理職業(yè)學(xué)院《高分子物理B》2023-2024學(xué)年第二學(xué)期期末試卷
- 鐵路冬季四防安全培訓(xùn)
- 2025水質(zhì)檢測技術(shù)服務(wù)合同
- 2025年高考?xì)v史歷史問答題5種公式法5種記憶法匯編
- 2025建筑工程施工合同范本2
- YS-T 3038-2020 黃金生產(chǎn)用顆粒活性炭
- 新生兒低蛋白血癥指南課件
- 四川省宜賓市2023-2024學(xué)年八年級上學(xué)期期末義務(wù)教育階段教學(xué)質(zhì)量監(jiān)測英語試題
- 電力各種材料重量表總
- 班級管理課件:班級文化管理
- 門窗工程工作總結(jié)報告
- (完整文檔版)CRF表
- 發(fā)展心理學(xué)第五章 幼兒的心理發(fā)展
- 廣東深圳市道路交通管理事務(wù)中心招考聘用員額制工作人員筆試歷年高頻考點試題含答案帶詳解
- 家長會課件:四下英語家長會優(yōu)質(zhì)課件
- 華文版書法五年級下冊 第10課 走之旁 教案

評論
0/150
提交評論