



版權說明:本文檔由用戶提供并上傳,收益歸屬內容提供方,若內容存在侵權,請進行舉報或認領
文檔簡介
氫化物發生原子吸收分析技術概述砷、銻、鉍、錫、鉛、硒、碲、鍺等元素的測定,其分析線都處于近紫外區,在常規火焰中多存在嚴重背景吸收,在石墨爐測定中基體干擾及灰化損失嚴重。這些元素在無機材料、食品及環境樣品中多屬有害成分,含量很低而且分析試樣的基體又往往很復雜。因此,采用原子吸收法進行分析經常必須加以分離或富集,方能達到分析的目的。而這些元素由于能生成容易揮發的氫化物,可以借此與基體分離。從而發展起了氫化物發生分析技術,可以集分離、富集和氣相進樣于一起的測試手段。溶液直接測定-火焰法100多年前Marsh曾利用不穩定的砷氫化物可在加熱的玻璃管壁上形成單質砷鏡的反應,創立了著名的馬氏試砷法。1969年W.Holak首先將砷氫化物生成法應用到原子吸收。此后許多學者將形成氫化物易于原子化的思路,用于砷、銻、鉍、錫、鉛、硒、碲、鍺等的測定。1982年I.S.Busheina等發現銦也能形成銦氫化物,1983年北京大學嚴杜等成功地將氫化物發生原子吸收法用于銦和鉈的測定。郭小偉等發現鎘也能用氫化物發生法測定。至今已見報道的可以測定的元素有汞、鋅、鎘、鍺、砷、銻、鉍、錫、鉛、硒、碲等。氫化物發生法在擴展元素應用范圍的同時,采用控制酸度選擇性的形成氫化物方法,還可用于形態分析。如控制酸度分別測定不同價態的銻,A.G.Howard等將此法用于無機砷Ⅲ,Ⅴ和甲基胂,二甲基胂等測定,1989年Cacho更將此法推廣用于揮發性鎘化合物的測定。至此表明,氫化物發生法不僅已發展成為原子吸收分析法的一個重要分支,而且為原子吸收方法的氣體進樣技術開拓了新的應用前景。氫化物發生法基本原理
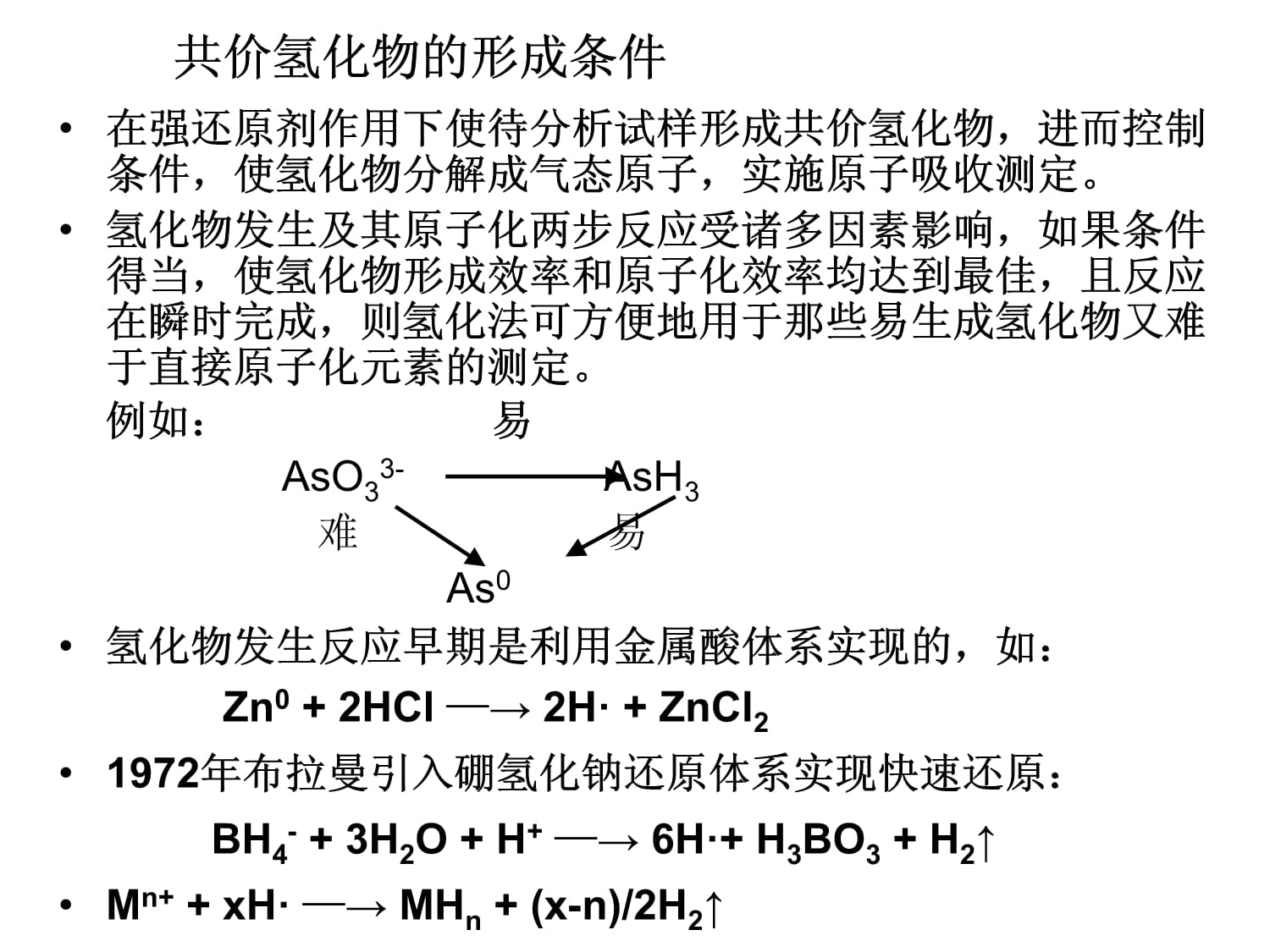
共價氫化物的形成條件1.硼氫化鈉還原體系2.反應液酸度3.氫化物的形成反應4.氫化物發生法形態分析5.氫化物生成速度問題6.還原劑加入順序和速度7.氫化物的傳輸8.氫化物發生裝置在強還原劑作用下使待分析試樣形成共價氫化物,進而控制條件,使氫化物分解成氣態原子,實施原子吸收測定。氫化物發生及其原子化兩步反應受諸多因素影響,如果條件得當,使氫化物形成效率和原子化效率均達到最佳,且反應在瞬時完成,則氫化法可方便地用于那些易生成氫化物又難于直接原子化元素的測定。例如:易
AsO33-AsH3
難易
As0氫化物發生反應早期是利用金屬酸體系實現的,如:
Zn0+2HCl—→2H·+ZnCl21972年布拉曼引入硼氫化鈉還原體系實現快速還原:
BH4-+3H2O+H+
—→6H·+H3BO3+H2↑Mn++xH·—→MHn+(x-n)/2H2↑共價氫化物的形成條件
目前氫化物發生法絕大多數均采用硼氫化鈉(鉀)還原體系進行測定。其化學反應式為:從化學平衡角度分析,足夠的量和NaBH4適宜的濃度是氫化物生成反應完全的保證,過量的NaBH4水解產生的H2,對氫化物分解反應不利。如表1所列出,文獻上的硼氫化鈉濃度條件,實際上已超過化學平衡的需要。但由于氫化物形成反應,通常在室溫下進行,氫化物的沸點很低,這個生成氣體共價氫化物的反應是能滿足分析要求的。參考相應氫化物的物理參數(見表2)
,欲使反應進行完全,與諸多因素有關。BH4-+3H2O+H+
→6H·+H3BO3+H2↑
Mn++xH·→MHn+(x-n)/2H2↑表1氫化物形成的NaBH4濃度范圍
元素NaB4濃度范圍樣品來源As>5%生物、環境、地質As2%~4%NBS標樣,水樣AsⅢ0.5%~5%人體腎、肝Bi>2%環境Bi1.5%~4%水Ge0.5%~5%水Sb2.5%~4%NBS標樣,水樣Sn4%標樣,果醬等Sn0.4%~5%湖水,海水Sn2%~8%地質Se1%~4%環境SeⅣ0.5%~1%人體腎、肝Se,As6%~8%腎、肝Te6%~8%硅酸巖Te2.5%~4%NBS標樣表2部分元素氣體氫化物的性質
元素氫化物熔點(℃)沸點(℃)水中溶解度(g/mL)分子式名稱砷AsH3Arsine-116.3-62.4696鉍BiH3Bismuthine-6733)16.8-鍺GeH4Germane-164.8-88.1不溶鉛PbH4Plumbane-135-13-銻SbH3Stibine-88-18.44100硒SeH2SeleniumHydride-65.7-41.337.7~68mg/ml錫SnH4Stannane-146-52.5-碲TeH2TelluriumHydride-51-4易溶1.硼氫化鈉還原體系硼氫化鈉溶液作為強還原劑具有提供新生態活潑氫的反應:
BH4-+3H2O+H+→6H·+H3BO3+H2↑同時也存在分解反應:
BH4-+3H2O+H+→H3BO3+4H2↑硼氫化鈉在酸性條件下分解很快,即使在pH4時也快速分解,為此常在其溶液中加入少許NaOH使之穩定,當然這樣也會影響其還原作用。在此體系中通過控制酸度、硼氫化鈉的濃度、加入量等條件可以達到定量及形態的測定。2.反應液酸度不同元素氫化物形成反應需要的適宜酸度是不同的,主要決定于生成反應的穩定常數和反應速度。酸度太低,反應不完全,且較緩慢;酸度過高,促使還原劑NaBH4大量分解,產生大量H2,且減少氫化物在原子化器中的停留時間。以砷為例,在NaBH4作用下還原生成氫化物的反應為:
As3++BH4-+3H2O→AsH3↑+H3BO3+2H++H2↑由上述反應可見,氫化物形成是在一定的酸度條件下進行的。不同樣品、不同元素、不同的反應裝置和條件,許多作者給出了不盡相似的反應酸度條件(見表3)。酸度講的是體系的酸度,反應過程要考慮為使NaBH4穩定而加入的NaOH。體系中加酸,還要考慮其氧化性和絡合作用的因素。
表3氫化物生成酸度范圍
元素酸度范圍樣品AsⅢ5-6mol/LHCl洗滌粉AsⅢ0.1~4mol/LHCl鋼、金屬、煤灰等AsV3~6mol/LHCl洗滌粉AsV0.5~4mol/LHCl鋼、金屬、煤灰等SbⅢ1.5~8mol/LHCl環境、水Sb>1mol/LHCl河泥Bi1~5mol/LHCl電銅Bi1~4mol/LHAc環境樣GeNaAc-HAc煤渣Sn0.4~1.4mo/LHCl淡水、海水Sn0.05~0.2mol/LHCl地質PbpH2水樣Se2~5mol/LHCl煤Te3~4mol/LHCl煤As,Sb1~4mol/LHCl冶金樣品Bi,Se冶金樣品Sn冶金樣品As,Bi,Te0.1%~10%HCl冶金樣品3.氫化物的形成反應氫化物形成反應是個氧化還原反應。部分元素氧化還原反應平衡方程式及其形成常數見下表:半反應平衡lgKAs3++3H++6e→AsH3-11.7Sb3++3H++6e→SbH3-15.3Bi3++3H++6e→BiH3-29.8GeO2+8H++8e→GeH4+2H2O-40Se4++2H++6e→H2Se37.4Te4++2H++6e→H2Te10.4Hg2++2e→Hg28.5砷、銻、鉍、鍺形成氫化物能力及其穩定性和分析靈敏度遞減
Se4+,Te4+在廣泛的酸性范圍內,極易生成H2Se及H2Te
氫化物穩定性不同:AsH3,SbH3很穩定,用儲氣富集法可提高靈敏度4.氫化物發生法形態分析周期表Ⅲ,Ⅳ,Ⅴ,Ⅵ主族元素有不同價態的存在形式,它們在強還原劑作用下發生氫化物反應的難易程度,生成速度和所需要反應條件均不盡相同。因而有可能控制不同反應條件分別測定不同價態或不同存在形式的分析。在相似還原條件下有些元素不同價態的信號比如:AsⅤ/AsⅢ=0.92,SbⅤ/SbⅢ=0.12,TeⅥ/TeⅣ=1.00。信號比的不同反映了元素價態之間性質的差異,提供可能控制影響因素,可以分別測定它們。Simemus在低酸度選擇性地測定SbⅢ,然后另取溶液加入還原劑KI,使SbⅤ還原為SbⅢ,測定總量后,差值即為高價銻濃度。Howard等采用選樣性氫化物發生AAS法測定AsⅢ?Ⅴ和甲基胂、二甲基胂體系。表明此法進行形態分析的可能性。
5.氫化物生成速度問題
硼氫化鈉作為還原劑,使氫化物發生技術產生了深刻變化,可使反應速度加快,而且生成效率高.絕大部分元素氫化物的生成反應,在NaBH4作用下是瞬時完成的。Sn,Pb等元素條件控制不當,有可能延緩反應。溫度是影響反應速度的重要因素。有文獻報道Pb,Te,Se等的靈敏度隨反應溫度升高而明顯下降。由于In和Tl氫化物極不穩定,相應氫化物生成受反應溫度影響很大。
6.還原劑加入順序和速度氫化法測定中,常規的操作順序為:
樣品→酸度調節→加還原劑→收集氫化物但在不同元素氫化物生成過程中,由于下列因素的影響使得何時加入還原劑及加入速度顯得十分重要。
(1)NaBH4還原反應和分解反應同時存在;
(2)氫化物的穩定性不同;
(3)共存元素的影響;
(4)氫化物的傳遞與原子化方式。氫化法測定中,要有利于還原劑與樣品的充分接觸,減少還原劑的損失以保證氫化物的生成效率。7.氫化物的傳輸
從溶液中釋放出的氫化物由載氣流送人原子化器或離子化器,當通過玻璃或塑料管時,由于氫化物的分解或被吸附會造成氫化物有一定量的損失,同時在氫化物發生器中存在的水也會增加氫化物的損失或延遲作用,原因是氫化物在水中有一定的溶解度(見表4)。這些因素使氫化物傳輸的效率降低,因而降低了測定靈敏度,更是破壞了測定的重復性。氫化物傳輸過程的損失,可在實驗裝置優化的前提下減小到可忽略不計的程度。優化過程包括選擇合理的載氣流速,減小傳輸途徑中的表面積。用細管傳送氫化物可明顯地減少氫化物與管壁的作用。
8.氫化物發生裝置
氫化物發生有直接傳遞模式和收集模式兩種(如圖2)直接模式:簡單的氫化物發生與原子吸收儀器的連接如下圖所示:連續流動模式有三種方法將氫化物直接送入原子化器或離子化器,即連續流動式(continuousflow,簡稱CF),流動注射式(flowinjection,簡稱FI)和批量間歇式(batch)。下圖為典型的流動形式:(1).連續流動氫化物發生器連續流動氫化物發生器的一般流路如圖,流速固定的試液和硼氫化物溶液與載氣混合,進入氣液分離器后,氣體與溶液分開,氣態氫化物同氫氣等與載氣一道進入原子化器或離子化器,廢液從下面排出。(2).流動注射氫化物發生器一般流動注射氫化物發生器如下簡圖,實驗順序與CF方法相似,所不同的是,在這里用固定流速的酸載流(fs)代替樣品流速。氫化物發生法的干擾及其消除1.氫化物發生的干擾類型氫化物原子吸收分析中所遇到的干擾現象很多,可以將其分為凝聚相干擾和氣相干擾兩種類型。凝聚相干擾:指干擾發生在氫化物生成時及氫化物從樣品溶液釋放的過程中。凝聚相干擾可能是氫化物生成速度的改變引起的,也可能是氫化物轉化率及釋放率的改變引起的。氣相干擾:指發生在氣相中的干擾,即這種干擾發生在氫化物傳輸過程中及原子化過程中。氣相干擾是揮發性干擾物引起的,可能是直接式的,也可能是記憶式的干擾。按干擾物來分,氫化物原子吸收分析中的干擾可分介質酸度干擾、氧化還原體系干擾、重金屬和貴金屬干擾及易形成共價氫化物元素干擾等四大類型。
2.氫化物發生的干擾機理(1)
形成固態氫化物:酸度不合適時既影響氫化物的生成速度,又容易產生固態氫化物或泡沫狀的衍生物。
(2)形成難溶化合物:待測元素與干擾元素之間生成難溶于酸的化合物,影響氫化物的釋放而引起負干擾。(3)析出金屬沉淀捕獲氫化物:某些金屬離子在酸性介質中可被硼氫化鈉還原成金屬而沉淀析出,新析出的金屬沉淀捕獲待測元素的氫化物而降低氫化物的釋放效率則導致負干擾。
(4)產生氧化性氣體:硝酸作為氧化劑而被樣品基體還原成亞硝酸根,亞硝酸根的分解引起干擾。(5)催化作用:被BH4-還原出的金屬作為摧化劑而影響BH4-與NO3-之間的反應,NO2-、NO2和NO的增多將引起嚴重的負干擾。(6)消耗氣相中的自由基:生成共價氫化物元素之間會產生氧化還原競爭而發生干擾,這類干擾屬于氣相干擾。(7)
價態效應:氫化物原子吸收法的靈敏度受待測元素的價態影響。若測定某種元素的總量或測定其中某一價態的含量,必須考慮價態效應,否則會引起較大的測定誤差。這些干擾的類型可采取相應的措施來消除和降低干擾。3.氫化物發生干擾的消除途徑(1)選擇最佳酸介質(2)選擇最佳還原劑濃度及用量(3)利用掩蔽作用文獻中有一系列掩蔽劑,如:EDTA,KI,KCN,檸檬酸、氨基硫脲、1,10-菲咯啉、KSCN、草酸、酒石酸、硫脲,吡啶-2-醛肟、連苯三酚,銅鐵靈,茜素氟藍等試劑已廣泛用來克服氫化物原子吸收分析中的干擾。
(4)預還原和冷阱捕集(5)共沉淀和浮選分離(6)電解和溶劑萃取分離(7)色譜分離(8)干擾消除方法氫化物發生法在元素測定中的應用1砷用靈敏線193.7/197.2nm檢出限范圍3~80ng/L
在大酸度下測定有價態問題重金屬干擾2銻用靈敏線217.6nm檢出限范圍0.1~0.3g/L
在大酸度下測定有價態問題重金屬干擾3鉍用靈敏線223.1nm檢出限范圍0.1~0.8g/L
在大酸度下測定無價態問題重金屬干擾4錫用靈敏線286.3nm檢出限范圍0.1~5g/L
在低酸度下測定有價態問題重金屬干擾5鉛用靈敏線
溫馨提示
- 1. 本站所有資源如無特殊說明,都需要本地電腦安裝OFFICE2007和PDF閱讀器。圖紙軟件為CAD,CAXA,PROE,UG,SolidWorks等.壓縮文件請下載最新的WinRAR軟件解壓。
- 2. 本站的文檔不包含任何第三方提供的附件圖紙等,如果需要附件,請聯系上傳者。文件的所有權益歸上傳用戶所有。
- 3. 本站RAR壓縮包中若帶圖紙,網頁內容里面會有圖紙預覽,若沒有圖紙預覽就沒有圖紙。
- 4. 未經權益所有人同意不得將文件中的內容挪作商業或盈利用途。
- 5. 人人文庫網僅提供信息存儲空間,僅對用戶上傳內容的表現方式做保護處理,對用戶上傳分享的文檔內容本身不做任何修改或編輯,并不能對任何下載內容負責。
- 6. 下載文件中如有侵權或不適當內容,請與我們聯系,我們立即糾正。
- 7. 本站不保證下載資源的準確性、安全性和完整性, 同時也不承擔用戶因使用這些下載資源對自己和他人造成任何形式的傷害或損失。
最新文檔
- 病案管理系統用戶使用手冊
- 2025二手設備采購合同
- 2025租房合同協議范本大全
- 2025年陽泉貨運從業資格仿真考題
- 寒假的一天日記250字左右
- 海普瑞內壓膜參數
- 彈簧串聯共振頻率
- 單韻母α的書寫順序
- 入學心得體會(15篇)
- 2025屆湖北省黃岡市黃梅縣育才高級中學高三核心模擬預測歷史試題(含答案)
- 檢驗科標本運送培訓
- 初中作文指導-景物描寫(課件)
- 秋 輕合金 鋁合金相圖及合金相課件
- 6.3.1 平面向量基本定理 課件(共15張PPT)
- 安全安全檢查表分析(SCL)記錄表(設備、設施)
- 城市濕地公園設計導則2017
- 小學巡課記錄表
- 消防管道隱蔽工程驗收報審表(表格記錄)
- 地質災害群測群防講義
- 高頻變壓器標準工時對照表
- 232425黃昆固體物理教案

評論
0/150
提交評論