



下載本文檔
版權說明:本文檔由用戶提供并上傳,收益歸屬內容提供方,若內容存在侵權,請進行舉報或認領
文檔簡介
廣東省云浮市蔡揚鳴中學高三化學下學期期末試卷含解析一、單選題(本大題共15個小題,每小題4分。在每小題給出的四個選項中,只有一項符合題目要求,共60分。)1.下列敘述正確的是A.1.00mol
NaCl中含有6.02×1023個NaCl分子B.1.00mol
NaCl中,所有Na+的最外層電子總數為8×6.02×1023C.欲配置1.00L,1.00mol.L-1的NaCl溶液,可將58.5gNaCl溶于1.00L水中D.電解58.5g熔融的NaCl,能產生22.4L氯氣(標準狀況)、23.0g金屬鈉參考答案:A2.下列關于元素周期表和元素周期律的說法正確的是A.ⅥA族元素的原子半徑越大,越容易得到電子B.IA族與VIIA族元素間能形成離子化合物也能形成共價化合物C.IA族元素的金屬性比ⅡA族元素的金屬性強D.原子最外層電子數為2的元素一定位于元素周期表中的ⅡA族參考答案:B解析:A.同族元素,從上到下,原子半徑逐漸增大,非金屬性逐漸減弱,所以,ⅥA族元素的原子半徑越小,越容易得到電子,錯誤;B.IA族與VIIA族元素間能形成離子化合物也能形成共價化合物,正確;C.同周期元素,從左到右,金屬性逐漸減弱,同周期中,IA族元素的金屬性比ⅡA族元素的金屬性強,錯誤;D.氦位于零族,最外層有2個電子,所以原子最外層電子數為2的元素一定位于元素周期表中的ⅡA族是錯誤的;選B。3.下列五種有色溶液與SO2作用均能褪色,其實質相同的是
(
)①品紅溶液;②酸性KMnO4溶液;③溴水;④滴有酚酞的NaOH溶液;⑤含I2的淀粉溶液。A、②③⑤B、①②③C、①②④D、③④⑤參考答案:A略4.某中學一實驗小組組裝了下列所示實驗裝置,能達到實驗目的的是(
)
參考答案:D略5.(2009·廣東卷)我國稀土資源豐富。下列有關稀土元素與的說法正確的是(
)A.與互為同位素B.與的質量數相同C.與是同一種核素D.與的核外電子數和中子數均為62參考答案:A與核內質子數相同,中子數不同,是同一元素的不同核素,即同位素關系,所以本題選A。6.在下列裝置中(都盛有0.1mol/LH2SO4溶液)Zn片腐蝕最快的是()A.
B.
C.參考答案:C考點:原電池和電解池的工作原理.專題:電化學專題.分析:電化學腐蝕較化學腐蝕快,金屬得到保護時,腐蝕較慢,作原電池正極和電解池陰極的金屬被保護,腐蝕快慢為:電解原理引起的腐蝕>原電池原理引起的腐蝕>化學腐蝕>有防護腐蝕措施的腐蝕.解答:解:A中發生化學腐蝕,B中鋅作原電池正極,鋅被保護,C中鋅作負極,發生電化學腐蝕,加快鋅的腐蝕,所以腐蝕速率由快到慢的順序為C>A>B,故選C.點評:本題考查不同條件下金屬腐蝕的快慢,明確腐蝕快慢為:電解原理引起的腐蝕>原電池原理引起的腐蝕>化學腐蝕>有防護腐蝕措施的腐蝕即可解答,題目難度不大.7.下列操作不能達到目的的是參考答案:B略8.有一未知的無色溶液,只可能含有以下離子中的若干種(忽略由水電離產生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,現取三份100mL溶液進行如下實驗:①第一份加足量AgNO3溶液后,有白色沉淀產生。②第二份加足量BaCl2溶液后,有白色沉淀產生,經洗滌、干燥后,沉淀質量為6.99g。③第三份逐滴滴加NaOH溶液,測得沉淀與NaOH溶液的體積關系如圖。根據上述實驗,以下推測不正確的是A.原溶液一定不存在H+、Cu2+、CO32-
B.不能確定原溶液是否含有K+、NO3-C.原溶液確定含Mg2+、Al3+、NH4+,且n(Mg2+):n(Al3+):n(NH4+)=1:1:2D.實驗所加的NaOH的濃度為2mol·L-1參考答案:B略9.對于可逆反應:mA(g)+nB(g)xC(g)
ΔH=?,在不同溫度及壓強(p1、p2)條件下,反應物A的轉化率如圖所示,下列判斷正確的是()A.ΔH>0,m+n>x
B.ΔH>0,m+n<xC.ΔH<0,m+n<x
D.ΔH<0,m+n>x參考答案:D略10.向CuSO4溶液中逐滴加入過量KI溶液,觀察到產生白色沉淀,溶液變為棕色。淀粉KI溶液中通入SO2氣體,溶液無明顯變化。則下列分析中正確的是
A.白色沉淀是CuI2,棕色溶液含有I2
B.滴加KI溶液時,轉移2mole-時生成1mol白色沉淀
C.通入SO2時,SO2與I—反應,I—作還原劑D.上述實驗條件下,物質的氧化性:Cu2+>I2>SO2參考答案:D略11.下列實驗能成功的是 ①用灼燒法鑒別Na2CO3固體和NaHCO3固體②用觀察法區別Na2O粉末和Na2O2粉末③用AlCl3溶液鑒別Na2CO3溶液和NaOH溶液④用澄清石灰水鑒別Na2CO3溶液和NaHCO3溶液A.全部
B.①②④ C.②③④ D.①②③參考答案:D12.2008年北京奧運會的國家游泳中心(水立方)的建筑采用了膜材料ETFE,該材料的結構簡式為[
CH2—CH2—CF2—CF2
]n,下列說法正確的是
()
A.合成ETFE的反應為縮聚反應
B.ETFE材料具有固定且較高的熔點
C.合成ETFE材料的單體為四氟乙烯和乙烯
D.ETFE分子與乙烯屬于同系物參考答案:答案:B13.下列離子方程式中,屬于水解反應的是()A.HCOOH+H2OHCOO-+H3O+
B.CO2+H2OHCO3-+H+C.CO32-+H2OHCO3-+OH-
D.HS-+H2OS2-+H3O+參考答案:C略14.在水溶液中,YO3n-和S2-發生如下反應:YO3n-
+3S2-+6H+=Y-+3S↓+3H2O,則YO3n-中Y元素的化合價和原子最外層電子數分別為
A.+4、6
B.+7、7
C.+5、7
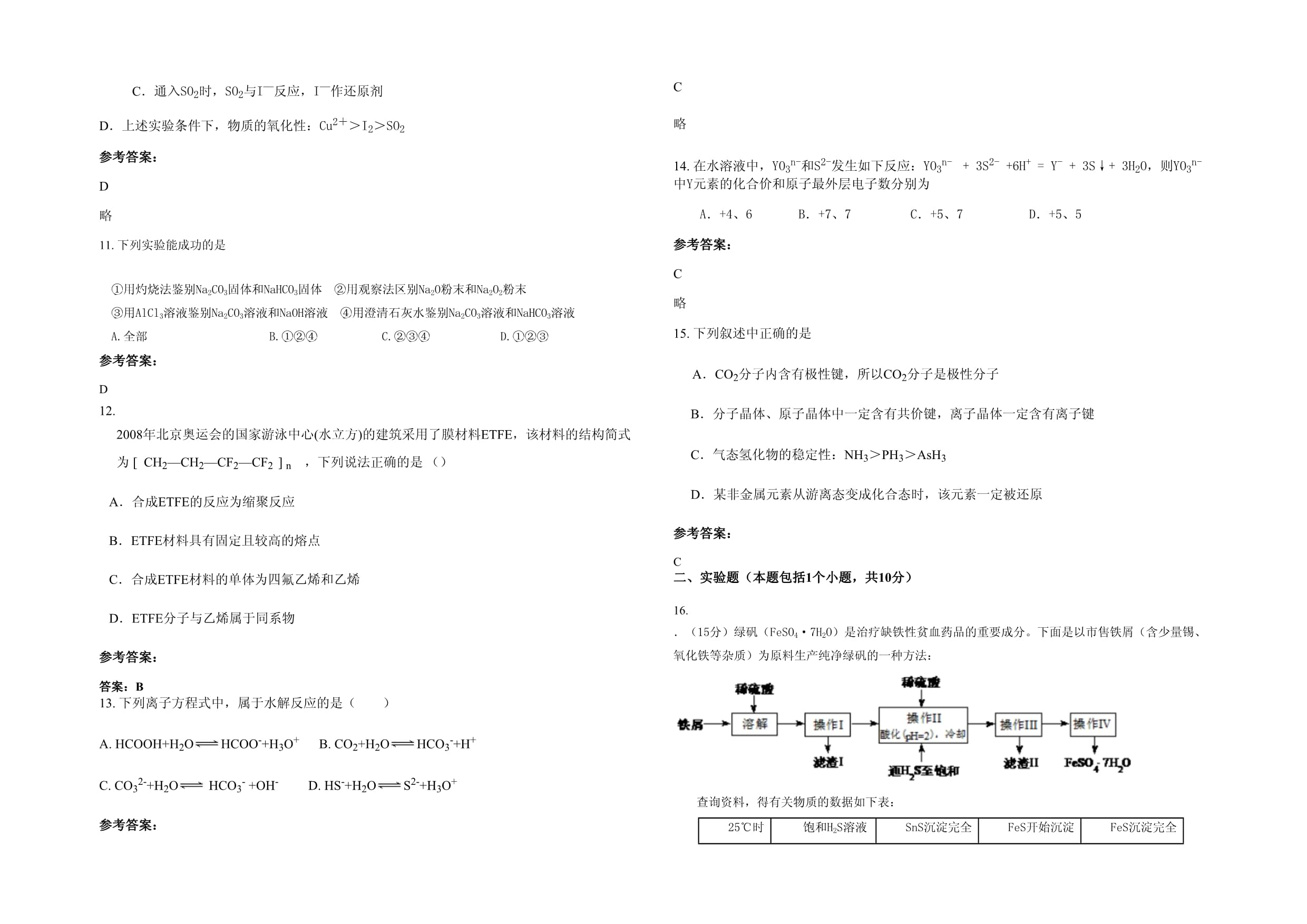
D.+5、5參考答案:C略15.下列敘述中正確的是A.CO2分子內含有極性鍵,所以CO2分子是極性分子B.分子晶體、原子晶體中一定含有共價鍵,離子晶體一定含有離子鍵C.氣態氫化物的穩定性:NH3>PH3>AsH3D.某非金屬元素從游離態變成化合態時,該元素一定被還原參考答案:C二、實驗題(本題包括1個小題,共10分)16..(15分)綠礬(FeSO4·7H2O)是治療缺鐵性貧血藥品的重要成分。下面是以市售鐵屑(含少量錫、氧化鐵等雜質)為原料生產純凈綠礬的一種方法:查詢資料,得有關物質的數據如下表:25℃時飽和H2S溶液SnS沉淀完全FeS開始沉淀FeS沉淀完全pH3.91.63.05.5(1)操作II中,通入硫化氫至飽和的目的是
;在溶液中用硫酸酸化至pH=2的目的是
。(2)析出的FeSO4·7H2O晶體通過如右圖所示裝置與母液分離。制作過濾器時,選擇比布氏漏斗內徑(選填“略大”、“略小”、“等大”)的濾紙,同時要求濾紙能。在減壓過濾中,先用法轉移溶液,(選填“開大”、“關小”)水龍頭,待溶液快流盡時再轉移沉淀。洗滌晶體時,應先(選填“開大”、“關小”、“關閉”)水龍頭,用冰水淋洗,其目的是:①除去晶體表面附著的硫酸等雜質;②
。(3)晶體中所含結晶水可通過重量分析法測定,主要步驟有:①稱量,②置于烘箱中脫結晶水,③
,④稱量,⑤重復②~④至恒重,⑥計算。請補充完整步驟③,步驟③需要在干燥器中進行,理由是
。(4)綠礬晶體中Fe2+含量的測定可用酸性KMnO4標準溶液滴定。①準確稱量4.0g綠礬晶體樣品,于250mL錐形瓶中,加入25mL2mol·L-1的H2SO4溶液,使樣品溶解,加熱至40~50℃。②向此溶液中加入2gZn粉和5mL2mol·L-1的H2SO4溶液,煮沸約10min。用KSCN溶液在點滴板上檢驗點滴液,若溶液不立刻變紅,則進行步驟③,如果立刻變紅,則應繼續煮沸幾分鐘。③將濾液過濾至另一個錐形瓶中,用10mL1mol·L-1的H2SO4溶液洗滌錐形瓶,將全部Fe2+轉移入錐形瓶中。用0.2mol·L-1標準KMnO4溶液滴定至溶液出現微紅色即為終點,讀出消耗液體體積10.00mL。(i)下列關于滴定過程中操作正確的是
。A.滴定管用蒸餾水洗滌后,即可裝入標準溶液B.KMnO4溶液置于酸式滴定管中,裝液后,把滴定管夾在滴定管夾上,輕輕轉動活塞,放出少量標準溶液,使尖嘴充滿標準溶液C.本實驗不需要指示劑。滴加最后一滴KMnO4溶液時,溶液變成淺紅色,立即記錄此時的體積D.接近終點時,需用蒸餾水沖洗瓶壁和滴定管尖端懸掛的液滴(ii)產品中Fe2+的質量分數為
。參考答案:(1)除去溶液中的Sn2+離子,并防止Fe2+被氧化(2分)防止Fe2+離子生成沉淀(1分)(2)略小將全部小孔蓋住傾析開大關小降低洗滌過程中FeSO4·7H2O的損耗(每空1分,共6分)(3)冷卻(1分)防止吸水(1分)(4)(i)B(1分)(ii)14%(2分)三、綜合題(本題包括3個小題,共30分)17.某同學從資料上查到以下反應A、B為中學常見單質,AO2、BO2是能使澄清石灰水變渾濁的氣體。回答下列問題:(1)元素A、B可形成化合物AB2,則A元素的原子結構示意圖為
,
AB2中的化學鍵是
(2)若反應中A和B的質量比為3:4,則n(KClO3):n(AO2)=
(3)已知:寫出AB2(l)在O2中完全燃燒的熱化學方程式為
參考答案:(1),(極性)共價鍵
(2)1:1(3)AB2(l)+3O2(g)=2BO2(g)+AO2(g)
△H=-1076.8kj/mol【Ks5u解析】(1)A、B為中學常見單質,AO2、BO2是能使澄清石灰水變渾濁的氣體。它們分別是二氧化碳和二氧化硫,元素A、B可形成化合物AB2則A是C,B是S,則A元素的原子結構示意圖為,非金屬元素原子形成共價鍵,AB2中的化學鍵是共價鍵;(2)若反應中A為C和B為S的質量比為3:4,物質的量之比=(3÷12):(4÷32)=2:1;依據原子守恒配平化學方程式得到;2KClO3+2C+S=2KCl+2CO2+SO2,得到n(KClO3):n(CO2)=1:1;(3)根據蓋斯定律,①+②×2-③得反應熱為-1076.8kJ/mol,所以AB2(l)在O2中完全燃燒的熱化學方程式為AB2(l)+3O2(g)=2BO2(g)+AO2(g)
△H=-1076.8kJ/mol。18.(12分)鋰被譽為“高能金屬”。工業上用硫酸與β-鋰輝礦(LiAlSi2O6和少量鈣鎂雜質)在一定條件下反應生成Li2SO4(以及MgSO4、硅鋁化合物等物質),進而制備金屬鋰,其生產流程如下:(1)用氧化物形式表示LiAlSi2O6的組成:
▲
。
(2)沉淀X主要成分為CaCO3和
▲
。(3)寫出鹽酸與Li2CO3反應的離子方程式:
▲
。(4)寫出電解熔融LiCl時陰極的電極反應式:
▲
。(5)流程中兩次使用了Na2CO3溶液,試說明前后濃度不同的原因:前者是
▲
;后者是
▲
。參考答案:(12分)(1)Li2O·Al2O3·4SiO2(2分)(2)Mg(OH)2(2分)(3)Li2CO3+2H+=2Li++H2O+CO2↑(2分)(4)Li++e-=Li(2分)(5)濃度過大會使部分Li+沉淀(2分)此時濃度大則有利于Li2CO3沉淀的生成(2分,其他合理答案均可)略19.在精制飽和食鹽水中加入碳酸氫銨可制備小蘇打(NaHCO3),并提取氯化銨作為肥料或進一步提純為工業氯化銨。 完成下列填空:33.寫出上述制備小蘇打的化學方程式。 ___________________________________________________________________34.濾出小蘇打后,母液提取氯化銨有兩種方法:①通入氨,冷卻、加食鹽,過濾②不通氨,冷卻、加食鹽,過濾 對兩種方法的評價正確的是_____________。(選填編號)a.①析出的氯化銨純度更高
b.②析出的氯化銨純度更高c.①的濾液可直接循環使用
d.②的濾液可直接循環使用35.提取的NH4Cl中含有少量Fe2+、SO42―。將產品溶解,加入H2O2,加熱至沸,再加入BaCl2溶液,過濾,蒸發結晶,得到工業氯化銨。加熱至沸的目的是_____________________________________
溫馨提示
- 1. 本站所有資源如無特殊說明,都需要本地電腦安裝OFFICE2007和PDF閱讀器。圖紙軟件為CAD,CAXA,PROE,UG,SolidWorks等.壓縮文件請下載最新的WinRAR軟件解壓。
- 2. 本站的文檔不包含任何第三方提供的附件圖紙等,如果需要附件,請聯系上傳者。文件的所有權益歸上傳用戶所有。
- 3. 本站RAR壓縮包中若帶圖紙,網頁內容里面會有圖紙預覽,若沒有圖紙預覽就沒有圖紙。
- 4. 未經權益所有人同意不得將文件中的內容挪作商業或盈利用途。
- 5. 人人文庫網僅提供信息存儲空間,僅對用戶上傳內容的表現方式做保護處理,對用戶上傳分享的文檔內容本身不做任何修改或編輯,并不能對任何下載內容負責。
- 6. 下載文件中如有侵權或不適當內容,請與我們聯系,我們立即糾正。
- 7. 本站不保證下載資源的準確性、安全性和完整性, 同時也不承擔用戶因使用這些下載資源對自己和他人造成任何形式的傷害或損失。
最新文檔
- 門窗保潔服務標準操作培訓
- 職工入場安全培訓課件
- 安徽省宿州市墉橋區2025-2026學年三上數學期末綜合測試模擬試題含解析
- 玩滑梯有秩序
- 口腔頜面部腫瘤護理
- 水電工程空間位置關系分析試題及答案
- 設計公司案例分析
- 經濟法專科課程試題及答案分析
- 多元化工程經濟復習試題及答案
- 超市店長管理營銷
- 2025年護士考試心理健康試題及答案
- 第6課 我國國家機構(教學設計)2023-2024學年八年級道德與法治下冊同步教學(河北專版)
- 人工智能設計倫理知到智慧樹章節測試課后答案2024年秋浙江大學
- 生物醫學電子學智慧樹知到期末考試答案章節答案2024年天津大學
- 2023年版一級建造師-水利工程實務電子教材
- 新中考考試平臺-考生端V2.0使用手冊
- 診所備案申請表格(衛健委備案)
- 水上交通事故報告書(英文)
- 第五章-連續結晶
- 人體生物等效性試驗病例報告表(Case Report Form)CRF表格范本
- (整理)年產380萬噸煉鋼生鐵車間或2000立方米高爐設計設計

評論
0/150
提交評論